题目内容
将CaO和Na2O两种碱性氧化物的混合物溶解于水,加入足量的K2CO3溶液充分应后过滤,得干燥的白沉淀,测得白色沉淀的质量与原混合物的质量相等.则原混合物中Na2O的质量分数为( )
| A、60% | B、56% |
| C、44% | D、40% |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:氧化钙和水反应生成氢氧化钙,氢氧化钙和碳酸钾反应生成了碳酸钙沉淀,根据题意可以知道反应后生成的碳酸钙的质量等于CaO和Na2O的质量,可以根据可以根据氧化钙和碳酸钙的关系得出它们的质量关系,然后求出解答即可.
解答:解:由CaO+H2O═Ca(OH)2
Ca(OH)2+CO2═CaCO3↓+H2O
得:CaO~CaCO3↓
56 100
56g 100g
由上式可以知道,56g氧化钙通过一系列反应后能够生成碳酸钙的质量为100g
根据上述分析可以知道若有56g氧化钙,则混合物的质量为100g
所以氧化钠的质量分数为:
×100%=44%
分析所给的选项可以知道选C正确.
故选C.
Ca(OH)2+CO2═CaCO3↓+H2O
得:CaO~CaCO3↓
56 100
56g 100g
由上式可以知道,56g氧化钙通过一系列反应后能够生成碳酸钙的质量为100g
根据上述分析可以知道若有56g氧化钙,则混合物的质量为100g
所以氧化钠的质量分数为:
| 100g-56g |
| 100g |
分析所给的选项可以知道选C正确.
故选C.
点评:解此类题时,要能够灵活的应用质量守恒定律,以及根据题中的数据找出等量关系解答.

练习册系列答案
 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
下列物质在氧气中燃烧时,能产生无色气体的是( )
| A、红磷 | B、木条 | C、铁丝 | D、镁带 |
为了保证某些玻璃仪器的密封性,常常把玻璃的接触面进行磨砂处理.下列仪器经过磨砂处理的是( )
| A、量筒 | B、广口瓶 | C、烧杯 | D、试管 |
下列关于碳的单质及其化合物的用途与其所依据的性质不相符合的是( )
| A、干冰用于人工降雨:干冰升华时吸热 |
| B、金刚石用于刻划玻璃:金刚石的硬度最大 |
| C、活性炭用作冰箱除臭剂:活性炭具有吸附性 |
| D、一氧化碳用于冶炼生铁:一氧化碳具有可燃性 |
下列化学用语正确的是( )
| A、铝的元素符号:Cl |
| B、五氧化二磷分子:P2O5 |
| C、硫酸铁:FeSO4 |
| D、镁离子:Mg+ |
甲、乙两种固体的溶解度曲线如图所示,下列说法正确的是( )
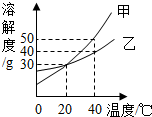

| A、乙中混有少量甲时,可以用冷却热饱和溶液的方法提纯乙 |
| B、40℃时,分别在100g水中加入50g甲、乙,所得溶液溶质质量分数相等 |
| C、20℃时,甲、乙两种物质的饱和溶液中溶质的质量相等 |
| D、40℃时,甲溶液中溶质的质量分数不一定大于乙溶液中溶质质量分数 |
下列气体既能用浓硫酸干燥又能用氢氧化钠固体干燥的是( )
| A、H2 |
| B、NH3 |
| C、SO2 |
| D、HCl |
下列不属于空气质量报告内容的是( )
| A、空气中二氧化硫的含量 |
| B、空气中可吸入颗粒物的含量 |
| C、空气中一氧化碳的含量 |
| D、空气中氧气的含量 |
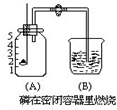 在空气中氧气含量的实验测定中,集气瓶中观察到的现象是:
在空气中氧气含量的实验测定中,集气瓶中观察到的现象是: