题目内容
2.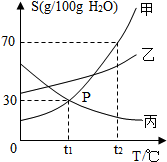 如图是甲、乙、丙三种物质(其晶体均不含结晶水)的溶解度曲线.据图回答:
如图是甲、乙、丙三种物质(其晶体均不含结晶水)的溶解度曲线.据图回答:(1)t1℃时甲的溶解度是40g.
(2)甲中含有少量的乙时,可通过降温结晶的方法提纯甲.
(3)将t2℃时甲、乙、丙三种物质的饱和溶液各100g,均降温到t1℃,则三种溶液中溶剂的质量大小关系正确的是D(填选项).
A.乙>甲=丙 B.甲=乙>丙 C.甲>乙>丙 D.丙>乙>甲
(4)若丙为氢氧化钙,向盛有饱和石灰水的烧杯中加入生石灰,溶液立即变浑浊,可能的原因是ABD(填字母).
A.生石灰与水反应的生成物不再溶解
B.反应放热,溶液温度升高,溶解度降低
C.空气中的二氧化碳与石灰水反应生成碳酸钙
D.生石灰与水反应消耗水,溶剂减少,有溶质析出.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,t1℃时甲的溶解度是40g;
(2)甲物质的溶解度受温度影响较大,所以甲中含有少量的乙时,可通过降温结晶的方法提纯甲;
(3)将t2℃时,甲物质的溶解度最大,乙物质的溶解度次之,丙物质的溶解度最小,甲、乙、丙三种物质的饱和溶液各100g,甲溶剂最多,乙溶剂次之,丙溶剂次之,均降温到t1℃,则三种溶液中溶剂的质量大小关系正确的是丙>乙>甲,故选:D;
(4)若丙为氢氧化钙,向盛有饱和石灰水的烧杯中加入生石灰,溶液立即变浑浊,
A、溶液是饱和溶液,生石灰与水反应的生成物不再溶解,故A正确;
B、反应放热,溶液温度升高,溶解度降低,氢氧化钙析出,故B正确;
C、空气中的二氧化碳与石灰水反应生成碳酸钙,变浑浊较快,故C错误;
D、生石灰与水反应消耗水,溶剂减少,有溶质析出,故D正确.
故选:ABD.
故答案为:(1)30g;
(2)降温结晶;
(3)D;
(4)ABD.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
13.在下列各种情况下,埋在地下的铸铁管道被腐蚀速率最慢的是( )
| A. | 在含砂粒较多、潮湿、透气的土壤中 | B. | 在干燥、致密、透气的土壤中 | ||
| C. | 在潮湿、疏松、透气的土壤中 | D. | 在呈酸性的潮湿土壤中 |
17.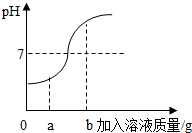 经过一年的学习,我们对“酸碱盐”有了一定的认识,请回答下列有关问题.
经过一年的学习,我们对“酸碱盐”有了一定的认识,请回答下列有关问题.
(1)下列说法中不正确的是B.
A、酸和碱中一定都含有氢元素
B、氯化钠由氯化钠离子构成
C、多数酸和碱都有腐蚀性
D、浓硫酸可用作某些气体的干燥剂
(2)在用稀盐酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的酸碱度变化如图所示,该图横坐标代表的是NaOH溶液的质量.当加入该溶液的质量为ag时,所得溶液中含量最多的溶质为(写化学式)NaCl.
(3)某敞口放置的氢氧化钠溶液已经变质,请用化学方程式表示其变质的原因.
(4)为了证明该瓶氢氧化钠溶液未完全变质,进行了以下实验,请将如表填写完整.
(5)现有部分变质的氢氧化钠样品18.6g与146g溶质质量分数为10%的盐酸溶液恰好完全反应生成CO24.4g,计算样品中NaOH的质量分数?
 经过一年的学习,我们对“酸碱盐”有了一定的认识,请回答下列有关问题.
经过一年的学习,我们对“酸碱盐”有了一定的认识,请回答下列有关问题.(1)下列说法中不正确的是B.
A、酸和碱中一定都含有氢元素
B、氯化钠由氯化钠离子构成
C、多数酸和碱都有腐蚀性
D、浓硫酸可用作某些气体的干燥剂
(2)在用稀盐酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的酸碱度变化如图所示,该图横坐标代表的是NaOH溶液的质量.当加入该溶液的质量为ag时,所得溶液中含量最多的溶质为(写化学式)NaCl.
(3)某敞口放置的氢氧化钠溶液已经变质,请用化学方程式表示其变质的原因.
(4)为了证明该瓶氢氧化钠溶液未完全变质,进行了以下实验,请将如表填写完整.
| 实验操作 | 现象 | 结论或化学方程式 |
| 取少量该样品,滴加足量的BaCl2溶液,过滤 | 有白色沉淀生成 | 方程式为:Na2CO3+BaCl2=BaCO3↓+2NaCl |
| 在滤液中滴加酚酞溶液 | 滤液显红色 | 样品未完全变质 |
14.KNO3属于( )
| A. | 钾肥 | B. | 磷肥 | C. | 氮肥 | D. | 复合肥 |
11. 下列各组物质中,存在如图所示的相互反应和转化关系的是( )
下列各组物质中,存在如图所示的相互反应和转化关系的是( )
 下列各组物质中,存在如图所示的相互反应和转化关系的是( )
下列各组物质中,存在如图所示的相互反应和转化关系的是( )| 选项 | 甲 | 乙 | 丙 | 丁 |
| A | O2 | CH4 | H2O | CO2 |
| B | C | Fe2O3 | Fe | CO2 |
| C | CuO | HCl | CuCl2 | H2O |
| D | CO2 | CaCl2 | CaCO3 | H2O |
| A. | A | B. | B | C. | C | D. | D |
12.NaOH、Na2CO3、NaCl在不同溶剂中的溶解度如表所示.
表1 NaOH、Na2CO3、NaCl分别在水中的溶解度(g)
表2 常温下,NaOH、Na2CO3、NaCl分别在乙醇中的溶解度(g)
根据表1和表2提供的数据回答下列问题:
(1)NaOH在水中的溶解度随温度升高而增大(填“增大”或“减小”).
(2)20℃时,饱和食盐水中溶质质量分数的计算式为$\frac{36g}{100g+36g}$×100%.
(3)小明同学将CO2通入饱和NaOH的乙醇溶液中,可观察到有白色固体析出的现象.
表1 NaOH、Na2CO3、NaCl分别在水中的溶解度(g)
| t/℃ | NaOH | Na2CO3 | NaCl |
| 0 | 42 | 7.1 | 35.7 |
| 10 | 51 | 12.2 | 35.8 |
| 20 | 109 | 21.8 | 36.0 |
| 30 | 119] | 39.7 | 36.3 |
| NaOH | Na2CO3 | NaCl |
| 17.3 | <0.01 | 0.1 |
(1)NaOH在水中的溶解度随温度升高而增大(填“增大”或“减小”).
(2)20℃时,饱和食盐水中溶质质量分数的计算式为$\frac{36g}{100g+36g}$×100%.
(3)小明同学将CO2通入饱和NaOH的乙醇溶液中,可观察到有白色固体析出的现象.
 如图所示是冶铁的反应原理,写出一氧化碳与氧化铁反应的现象固体由红棕色变化为黑色,反应方程式是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,图中右边酒精的作用是点燃没有参与反应的CO.
如图所示是冶铁的反应原理,写出一氧化碳与氧化铁反应的现象固体由红棕色变化为黑色,反应方程式是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,图中右边酒精的作用是点燃没有参与反应的CO.