题目内容
17. 经过一年的学习,我们对“酸碱盐”有了一定的认识,请回答下列有关问题.
经过一年的学习,我们对“酸碱盐”有了一定的认识,请回答下列有关问题.(1)下列说法中不正确的是B.
A、酸和碱中一定都含有氢元素
B、氯化钠由氯化钠离子构成
C、多数酸和碱都有腐蚀性
D、浓硫酸可用作某些气体的干燥剂
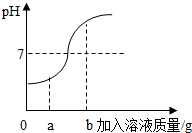
(2)在用稀盐酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的酸碱度变化如图所示,该图横坐标代表的是NaOH溶液的质量.当加入该溶液的质量为ag时,所得溶液中含量最多的溶质为(写化学式)NaCl.
(3)某敞口放置的氢氧化钠溶液已经变质,请用化学方程式表示其变质的原因.
(4)为了证明该瓶氢氧化钠溶液未完全变质,进行了以下实验,请将如表填写完整.
| 实验操作 | 现象 | 结论或化学方程式 |
| 取少量该样品,滴加足量的BaCl2溶液,过滤 | 有白色沉淀生成 | 方程式为:Na2CO3+BaCl2=BaCO3↓+2NaCl |
| 在滤液中滴加酚酞溶液 | 滤液显红色 | 样品未完全变质 |
分析 (1)A、根据酸在水溶液中会电离出氢离子,碱在水溶液中会电离出氢氧根离子进行分析;
B、根据氯化钠由钠离子、氯离子构成的进行分析;
C、根据多数酸和碱都有腐蚀性进行分析;
D、根据浓硫酸具有吸水性进行分析;
(2)根据图象中pH值的变化情况进行分析;
(3)根据氢氧化钠和二氧化碳反应生成碳酸钠和水进行分析;
(4)根据检验碳酸钠的变质情况,先加氯化钡或氯化钙检验是否含有碳酸钠,然后加酚酞检验是否含有氢氧化钠进行分析;
(5)根据碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,依据二氧化碳的质量计算出碳酸钠,然后计算氢氧化钠的质量分数进行分析.
解答 解:(1)A、酸在水溶液中会电离出氢离子,碱在水溶液中会电离出氢氧根离子,所以酸和碱中一定都含有氢元素,故A正确;
B、氯化钠由钠离子、氯离子构成的,故B错误;
C、多数酸和碱都有腐蚀性,故C正确;
D、浓硫酸具有吸水性,故D正确;
故选:B;
(2)由图象中pH值的变化情况可知,开始溶液的pH值小于,然后随着另一种溶液的加入,溶液的pH值逐渐的增大到7,然后大于7,所以该图横坐标代表的是NaOH溶液的质量,当加入该溶液的质量为ag时,所得溶液中含量最多的溶质为NaCl;
(3)氢氧化钠和二氧化碳反应生成碳酸钠和水,化学方程式为:2NaOH+CO2=Na2CO3+H2O;
(4)检验碳酸钠的变质情况,先加氯化钡或氯化钙检验是否含有碳酸钠,然后加酚酞检验是否含有氢氧化钠,所以
| 实验操作 | 现象 | 结论或化学方程式 |
| 取少量该样品,滴加足量的BaCl2溶液,过滤 | 有白色沉淀生成 | 方程式为:Na2CO3+BaCl2=BaCO3↓+2NaCl |
| 在滤液中滴加酚酞溶液 | 滤液显红色 | 样品未完全变质 |
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 4.4g
$\frac{106}{x}$=$\frac{44}{4.4g}$
x=10.6g
所以样品中NaOH的质量分数为:$\frac{18.6g-10.6g}{18.6g}$×100%=43%.
故答案为:(1)B;
(2)NaOH,NaCl;
(3)2NaOH+CO2=Na2CO3+H2O;
(4)BaCl2(或CaCl2),Na2CO3+BaCl2=BaCO3↓+2NaCl,滤液显红色;
(5)43%.
点评 本题主要考查了酸碱中和反应中的相关知识和化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.下列人体必需元素中,属于微量元素的是( )
| A. | 氢 | B. | 钙 | C. | 锌 | D. | 氧 |
7. 某电镀厂的电镀液中含有金盐,为了回收单质金,制作了如图所示的“吸金球”,“吸金球”是将某种“吸金”物质装进纱袋,做成球状.将“吸金球”放入电镀液中,便会发生神奇的化学反应.综上所述,“吸金球”中的“吸金”物质可能是( )
某电镀厂的电镀液中含有金盐,为了回收单质金,制作了如图所示的“吸金球”,“吸金球”是将某种“吸金”物质装进纱袋,做成球状.将“吸金球”放入电镀液中,便会发生神奇的化学反应.综上所述,“吸金球”中的“吸金”物质可能是( )
 某电镀厂的电镀液中含有金盐,为了回收单质金,制作了如图所示的“吸金球”,“吸金球”是将某种“吸金”物质装进纱袋,做成球状.将“吸金球”放入电镀液中,便会发生神奇的化学反应.综上所述,“吸金球”中的“吸金”物质可能是( )
某电镀厂的电镀液中含有金盐,为了回收单质金,制作了如图所示的“吸金球”,“吸金球”是将某种“吸金”物质装进纱袋,做成球状.将“吸金球”放入电镀液中,便会发生神奇的化学反应.综上所述,“吸金球”中的“吸金”物质可能是( )| A. | 铁屑(Fe) | B. | 胆矾(CuSO4•5H2O) | ||
| C. | 活性炭(C) | D. | 磁石(主要成分Fe3O4) |
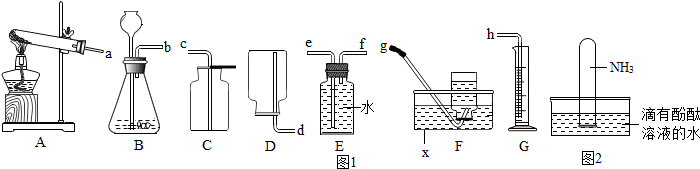
 A、B、C属于不同类别的化合物,分别和食盐含有一种相同元素,且它们发生的反应均属于复分解反应.“-”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质,一种A与B反应有气体放出,请写出A、B、C的化学式:ANa2CO3;BHCl;CNaOH.
A、B、C属于不同类别的化合物,分别和食盐含有一种相同元素,且它们发生的反应均属于复分解反应.“-”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质,一种A与B反应有气体放出,请写出A、B、C的化学式:ANa2CO3;BHCl;CNaOH.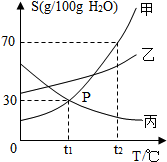 如图是甲、乙、丙三种物质(其晶体均不含结晶水)的溶解度曲线.据图回答:
如图是甲、乙、丙三种物质(其晶体均不含结晶水)的溶解度曲线.据图回答: