题目内容
根据以下装置回答下列问题
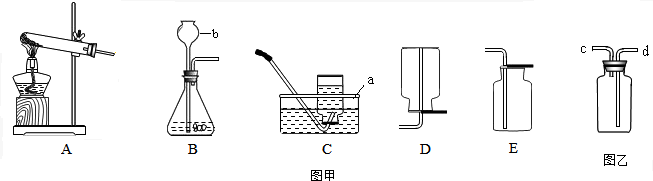
(1)写出标有字母仪器的名称:a b .在实验时,若发现酒精灯里有足量的酒精,却不能点燃,其可能原因是 .
(2)用高锰酸钾制氧气的化学方程式为 ,用A和C装置进行实验时,发现C中的水变成紫红色,原因是 .
(3)硫化氢(H2S)是一种具有臭鸡蛋气味的有毒气体,密度比空气大,易溶于水,其水溶液为氢硫酸,实验室用块状固体与稀硫酸反应来制取,实验室制H2S气体的发生装置是 (填字母).若用如图装置收集氨气,气体从 端导气管进入瓶中(填字母).收集的尾气应选择用 吸收(A、H2O、B、NaOH溶液C、H2SO4溶液)

(1)写出标有字母仪器的名称:a
(2)用高锰酸钾制氧气的化学方程式为
(3)硫化氢(H2S)是一种具有臭鸡蛋气味的有毒气体,密度比空气大,易溶于水,其水溶液为氢硫酸,实验室用块状固体与稀硫酸反应来制取,实验室制H2S气体的发生装置是
考点:氧气的制取装置,氧气的收集方法,制取氧气的操作步骤和注意点,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)要熟悉实验室常用仪器的名称和用途;
(2)据高锰酸钾制取氧气的反应原理书写方程式,加热时试管口要放一团棉花,防止高锰酸钾粉末进入导管;
(3)据反应物状态和反应条件选择发生装置,硫化氢的密度比空气大,故用向上排空气法收集,氨气密度比空气小,应用向下排空气法收集,溶于水显碱性,应用酸性溶液吸收.
(2)据高锰酸钾制取氧气的反应原理书写方程式,加热时试管口要放一团棉花,防止高锰酸钾粉末进入导管;
(3)据反应物状态和反应条件选择发生装置,硫化氢的密度比空气大,故用向上排空气法收集,氨气密度比空气小,应用向下排空气法收集,溶于水显碱性,应用酸性溶液吸收.
解答:解:(1)a是水槽,b是可以加入液体的仪器长颈漏斗;正确使用酒精灯的方法是用完后,随时将灯冒盖上,否则由于酒精的挥发性,会导致灯心留有水分不易点燃;
(2)加热高锰酸钾制氧气同时生成锰酸钾、二氧化锰和氧气,化学方程式为2KMnO4?K2MnO4+MnO2+O2↑,用A和C装置进行实验时,发现水槽中的水变成紫红色,原因是试管口没有塞一小团棉花,造成在加热时一部分高锰酸钾粉末通过导管进入水槽,导致水槽中的水变红色;
(3)用块状固体与稀硫酸反应来制取硫化氢气体,属于固体和液体常温反应制取气体,故选发生装置B;氨气的相对分子质量是17<29,密度比空气小,应用向下排空气法收集,溶于水显碱性,应用酸性溶液反应进行吸收;
故答案为:(1)水槽;长颈漏斗;酒精灯不用时没有盖上灯帽致灯芯留有水份;
(2)2KMnO4
K2MnO4+MnO2+O2↑;试管口没有塞一小团棉花,造成高锰酸钾粉末通过导管进入水槽;
(3)B;c;C.
(2)加热高锰酸钾制氧气同时生成锰酸钾、二氧化锰和氧气,化学方程式为2KMnO4?K2MnO4+MnO2+O2↑,用A和C装置进行实验时,发现水槽中的水变成紫红色,原因是试管口没有塞一小团棉花,造成在加热时一部分高锰酸钾粉末通过导管进入水槽,导致水槽中的水变红色;
(3)用块状固体与稀硫酸反应来制取硫化氢气体,属于固体和液体常温反应制取气体,故选发生装置B;氨气的相对分子质量是17<29,密度比空气小,应用向下排空气法收集,溶于水显碱性,应用酸性溶液反应进行吸收;
故答案为:(1)水槽;长颈漏斗;酒精灯不用时没有盖上灯帽致灯芯留有水份;
(2)2KMnO4
| ||
(3)B;c;C.
点评:本题包含了丰富的实验基本技能知识,主要考查了装置选取,原理等,不仅要求学生熟悉实验仪器,而且要求学生对实验原理有较深刻的认识和理解,对于实验中出现的现象能做出正确的分析,能培养学生灵活解决问题的能力.

练习册系列答案
相关题目