题目内容
12.物质的用途与其性质密切相关.(1)铜常用于制作导线,因为其有良好的延展性和导电性.
(2)氢氧化钙常用于建筑材料,因为其吸收二氧化碳变成坚固的碳酸钙.其反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O.
(3)NaHCO3用于治疗胃酸(主要成分是盐酸)过多,其原因是(用化学方程式表示)NaHCO3+HCl=NaCl+H2O+CO2↑
(4)硬水中含有较多的Ca2+、Mg2+填离子符号,硬水软化的方法有蒸馏、煮沸.
分析 (1)根据金属的物理性质进行分析;
(2)根据二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水进行分析;
(3)根据碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳进行分析;
(4)根据硬水中含有较多的可溶性钙镁化合物,硬水软化的方法有煮沸、蒸馏进行分析.
解答 解:(1)铜常用于制作导线,主要利用的是其延展性和导电性;
(2)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,所以氢氧化钙吸收二氧化碳变成坚固的碳酸钙,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
(3)碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑;
(4)硬水中含有较多的可溶性钙镁化合物,硬水软化的方法有煮沸、蒸馏.
故答案为:(1)导电;
(2)碳酸钙,Ca(OH)2+CO2=CaCO3↓+H2O;
(3)NaHCO3+HCl=NaCl+H2O+CO2↑;
(4)Ca2+、Mg2+,煮沸、蒸馏.
点评 本题考查的是常见的物质的应用以及化学方程式的书写,完成此题,可以依据已有的物质的性质以及化学方程式的书写方法进行.

练习册系列答案
相关题目
2.某氮的氧化物中,氮元素与氧元素的质量比为7:16,则该氧化物中氮元素的化合价( )
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
20.在CuO和Fe粉的混合物中加入一定量的稀硫酸,微热,待反应停止后过滤,滤出不溶物后再往滤液里加入一枚铁钉,若铁钉产生气泡,则叙述错误的是( )
| A. | 不溶物中一定有铜 | |
| B. | 不溶物中可能有铁 | |
| C. | 滤液可能是硫酸铜、硫酸亚铁的硫酸的混合溶液 | |
| D. | 不溶物的质量不可能与原混合物质量相等 |
7.生活中常常可以用化学知识来解决一些问题,下列家庭小实验不合理的是( )
| A. | 用食醋除去暖水瓶中的薄层水垢 | |
| B. | 用灼烧并闻气味的方法区别纯棉织物和纯毛织物 | |
| C. | 用食用碱(Na2CO3)溶液洗涤餐具上的油污 | |
| D. | 用米汤检验碘酸钾(KIO3) |
4.下列由实验事实或信息所得出的结论正确的是( )
| A. | 加压时25立方米的石油气可装入体积为0.024立方米的钢瓶中--分子在不停的运动 | |
| B. | 降低温度时某溶液中有晶体析出--该溶液降温前一定是饱和溶液 | |
| C. | 常温时某溶液能使酚酞溶液变红--该溶液一定是碱的溶液 | |
| D. | 某物质在空气中燃烧后生成二氧化碳和水--该物质中一定含有C、H元素 |
 下图表示电解水的简易装置.回答下列问题:
下图表示电解水的简易装置.回答下列问题: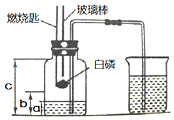 某科学兴趣小组的同学在学习了空气中氧气含量的测定的基础上,改进了教材中的实验,设计出了如图所示的实验装置.实验步骤如下:
某科学兴趣小组的同学在学习了空气中氧气含量的测定的基础上,改进了教材中的实验,设计出了如图所示的实验装置.实验步骤如下: