题目内容
9.溶液是一种重要的混合物,下列有关溶液的说法正确的是( )| A. | 将食盐加入水中,所得溶液的质量与加入的食盐和水的总质量一定相等 | |
| B. | 洗涤剂能够洗涤油污是因为洗涤剂能够溶解油污 | |
| C. | 不饱和溶液通过降低温度一定能变成饱和溶液 | |
| D. | 25℃时,将某KNO3溶液蒸发10克水析出a克晶体,再蒸发10克水析出b克晶体,a与b的质量不一定相等 |
分析 A、根据溶液是由溶质和溶剂组成的,但当溶液达到饱和状态后,溶液的质量不再改变,进行分析判断;
B、洗涤剂能够洗涤油污是因为洗涤剂具有乳化作用;
C、根据不饱和溶液与饱和溶液之间的转化,进行分析判断;
D、根据硝酸钾溶液蒸发溶剂前,是否饱和考虑.
解答 解:A、溶液是由溶质和溶剂组成的,将食盐加入水中,但当溶液达到饱和状态后,溶液的质量不再改变,所得溶液的质量与加入的食盐和水的总质量不一定相等,故错误;
B、洗涤剂能够洗涤油污是因为洗涤剂具有乳化作用,错误;
C、不饱和溶液通过降低温度不一定能变成饱和溶液,如氢氧化钙的溶解度随着温度的降低而减小,其饱和溶液降低温度后,溶解度增大,溶液仍为不饱和溶液,故选项说法错误;
D、如果硝酸钾溶液蒸发溶剂前,是饱和溶液,蒸发10克水析出a克晶体,再蒸发10克水析出b克晶体,a与b的质量一定相等,如果硝酸钾溶液蒸发溶剂前,是不饱和溶液,蒸发10克水析出a克晶体,再蒸发10克水析出b克晶体,a与b的质量一定不相等,故D说法错误.
故选D.
点评 本题难度不大,可依据已有的知识解答.

练习册系列答案
相关题目
20.某兴趣小组的同学为了探究化学反应前后反应物与生成物之间的质量关系设计了如下三个实验:
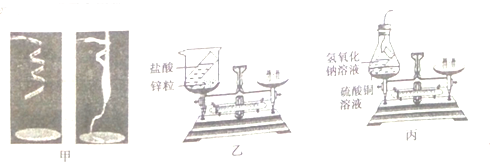
实验甲:称量镁条,在空气中点燃,待反应结束后,将生成物全部收回再称量.
实验乙:将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与锌粒接触,过一会再称量.(化学方程式是:Zn+2HCl=ZnCl2+H2↑)
实验丙:将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥形瓶口塞上橡皮塞,称量,然后设法将两种溶液接触,过一会再称量.(化学方程式是:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4)
他们得到三次实验的数据如表:
(1)在实验甲中反应后的质量比反应前明显增加了,请解释原因:镁燃烧时,和空气中的氧气反应生成了氧化镁,因此氧化镁的质量大于反应的镁的质量.
(2)由上表中数据分析可知实验甲中参加反应的氧气质量为3.2g,实验乙中生成氢气的质量为0.2g.
(3)在上述三个实验中都遵循(填“遵循”或者“不遵循”)质量守恒定律,但只有实验丙正确反映了反应物与生成物之间的总质量关系,因此,用实验来探究化学反应前后反应物与生成物之间的总质量关系时,当有气体参加或生成时,必须在密闭容器中进行.
(4)请从分子、原子的角度解释反应前后质量相等的原因:反应前后原子的种类、总个数、质量都不变.
(5)在化学反应前后,肯定不会变化的是①③④.
①原子的数目 ②分子的数目 ③元素的种类 ④物质的质量总和 ⑤物质的种类 ⑥物质的体积 ⑦物质的状态
(6)质量守恒定律这条结论的获得对化学研究的重大意义在于可以定量进行化学反应.

实验甲:称量镁条,在空气中点燃,待反应结束后,将生成物全部收回再称量.
实验乙:将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与锌粒接触,过一会再称量.(化学方程式是:Zn+2HCl=ZnCl2+H2↑)
实验丙:将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥形瓶口塞上橡皮塞,称量,然后设法将两种溶液接触,过一会再称量.(化学方程式是:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4)
他们得到三次实验的数据如表:
| 编号 | 实验甲 | 实验乙 | 实验丙 |
| 反应前/g | 4.8 | 112.6 | 118.4 |
| 反应后/g | 8.0 | 112.4 | 118.4 |
(2)由上表中数据分析可知实验甲中参加反应的氧气质量为3.2g,实验乙中生成氢气的质量为0.2g.
(3)在上述三个实验中都遵循(填“遵循”或者“不遵循”)质量守恒定律,但只有实验丙正确反映了反应物与生成物之间的总质量关系,因此,用实验来探究化学反应前后反应物与生成物之间的总质量关系时,当有气体参加或生成时,必须在密闭容器中进行.
(4)请从分子、原子的角度解释反应前后质量相等的原因:反应前后原子的种类、总个数、质量都不变.
(5)在化学反应前后,肯定不会变化的是①③④.
①原子的数目 ②分子的数目 ③元素的种类 ④物质的质量总和 ⑤物质的种类 ⑥物质的体积 ⑦物质的状态
(6)质量守恒定律这条结论的获得对化学研究的重大意义在于可以定量进行化学反应.
17.下列数据是硝酸钾和氯化钠在不同温度时的溶解度.
(1)30℃时,向l00g水中加入45.8g硝酸钾,充分溶解后得到饱和(选填“饱和”或“不饱和”)溶液.
(2)从NaCl溶液中得到NaCl晶体的方法是蒸发溶剂.
(3)从表中数据看,40℃时,氯化钠的溶解度与硝酸钾的溶解度相比更小(填“无法确定”“更大”“更小”).
(4)如图所示,小烧杯中盛放的是上述(1)中所得的硝酸钾溶液.若将少量的下列物质,分别小心地加入到大烧杯的水中,不断搅拌,一定能够使小烧杯中有固体析出的是AC(填字母).
A.冰 B.浓硫酸 C.硝酸铵 D.氢氧化钠.

| 温度/℃ | 10 | 30 | 50 | 60 | |
| 溶解度/g | 氯化钠 | 35.8 | 36.3 | 37.0 | 37.3 |
| 硝酸钾 | 20.9 | 45.8 | 85.5 | 110 | |
(2)从NaCl溶液中得到NaCl晶体的方法是蒸发溶剂.
(3)从表中数据看,40℃时,氯化钠的溶解度与硝酸钾的溶解度相比更小(填“无法确定”“更大”“更小”).
(4)如图所示,小烧杯中盛放的是上述(1)中所得的硝酸钾溶液.若将少量的下列物质,分别小心地加入到大烧杯的水中,不断搅拌,一定能够使小烧杯中有固体析出的是AC(填字母).
A.冰 B.浓硫酸 C.硝酸铵 D.氢氧化钠.
4.下列不能正确反映相关实验过程中量的变化关系的图象是( )
| A. |  分别向等质量Fe和Al中加入足量的溶质质量分数的稀盐酸 | |
| B. |  一定压强下,氧气在水中的溶解度 | |
| C. |  一定温度下,向不饱和硝酸钾溶液中加入硝酸钾 | |
| D. |  氯酸钾和二氧化锰混合加热制氧气中,a使用催化剂,b未使用催化剂 |
14.下列四个图象中有关量的变动趋势与对应的叙述关系中正确的是( )
| A. | 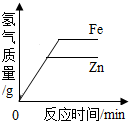 表示等质量的锌和铁分别与足量溶质质量分数相同的稀硫酸反应 | |
| B. | 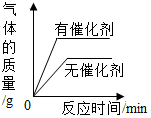 表示完全相同的两份过氧化氢溶液在有、无催化剂条件下的分解 | |
| C. | 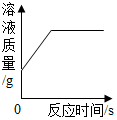 表示向一定量硫酸铜溶液中加入一定量锌粉 | |
| D. | 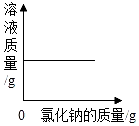 表示向一定量的饱和氯化钠溶液中加入硝酸钾固体 |


 在现代农业园,同学们学习到以下知识:
在现代农业园,同学们学习到以下知识: 如图中的物质为初中化学常见物质,他们之间的反应关系如图所示(“→”表示转化关系,“-”表示相互能反应,部分反应物、生成物或反应条件已略去).人的胃液中含有少量的A可帮助消化,A、B发生中和反应,产物之一是厨房内常用的调味品;C常用于改良酸性土壤,D为碳酸盐,且C的溶液与D的溶液反应可得到B;F和G在常温下都为气体.请回答:
如图中的物质为初中化学常见物质,他们之间的反应关系如图所示(“→”表示转化关系,“-”表示相互能反应,部分反应物、生成物或反应条件已略去).人的胃液中含有少量的A可帮助消化,A、B发生中和反应,产物之一是厨房内常用的调味品;C常用于改良酸性土壤,D为碳酸盐,且C的溶液与D的溶液反应可得到B;F和G在常温下都为气体.请回答: