题目内容
4.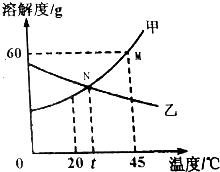 如图是甲、乙两物溶解度曲线.
如图是甲、乙两物溶解度曲线.(1)N点表示的意义是t℃时,甲、乙两物质溶解度相同;
(2)M点表示的意义是45℃时,甲的溶解度是60g;
(3)45℃时,在50g水中加入25g甲物质,形成的溶液为不饱和溶液(填“饱和溶液”或“不饱和溶液”),此时溶质、溶剂、溶液的质量比为1:2:3,溶质的质量分数为33.3%.
分析 根据题目信息和溶解度曲线可知:(1)甲、乙两种固体物质的溶解度,甲是随温度升高而增大;乙是随温度升高而减小;t℃时,甲、乙有交点,因此两物质溶解度相同;(2)45℃时,甲的溶解度是60g;(3)在一定的温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液是饱和溶液;45℃时,甲的溶解度是60g,即在100g水中加入60g甲,恰好形成饱和溶液,那么在50g水中加入30g甲物质,恰好形成饱和溶液,据此分析解答.
解答 解:根据题目信息和溶解度曲线可知:
(1)N点表示的意义是:t℃时,甲、乙有交点,因此两物质溶解度相同;
(2)M点表示的意义是:45℃时,甲的溶解度是60g;
(3)45℃时,甲的溶解度是60g,即在100g水中加入60g甲,恰好形成饱和溶液,那么在50g水中加入30g甲物质,恰好形成饱和溶液,因此,45℃时,在
50g水中加入25g甲物质,形成的溶液为不饱和溶液;此时溶质、溶剂、溶液的质量比为:25g:50g:(25g+50g)=1:2:3;此时溶液中溶质的质量
分数=$\frac{25g}{25g+50g}$×100%=33.3%.
故答案为:
(1)t℃时,甲、乙两物质溶解度相同;
(2)45℃时,甲的溶解度是60g;
(3)不饱和溶液;1:2:3;33.3%.
点评 本题考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液、溶质和溶剂的关系,还考查了有关点的意义,有关的计算要准确,本考点主要出现在选择题和填空题中.

练习册系列答案
相关题目
9. 乙醇是一种有机物,俗称酒精,在常温、常压下是一种易燃、易挥发的无色透明液体,它的水溶液具有酒香的气味,并略带刺激.乙醇的用途很广,可用乙醇制造醋酸、饮料、香精、染料、燃料等.乙醇的分子结构模型如图所示,下列有关乙醇的说法正确的是( )
乙醇是一种有机物,俗称酒精,在常温、常压下是一种易燃、易挥发的无色透明液体,它的水溶液具有酒香的气味,并略带刺激.乙醇的用途很广,可用乙醇制造醋酸、饮料、香精、染料、燃料等.乙醇的分子结构模型如图所示,下列有关乙醇的说法正确的是( )
 乙醇是一种有机物,俗称酒精,在常温、常压下是一种易燃、易挥发的无色透明液体,它的水溶液具有酒香的气味,并略带刺激.乙醇的用途很广,可用乙醇制造醋酸、饮料、香精、染料、燃料等.乙醇的分子结构模型如图所示,下列有关乙醇的说法正确的是( )
乙醇是一种有机物,俗称酒精,在常温、常压下是一种易燃、易挥发的无色透明液体,它的水溶液具有酒香的气味,并略带刺激.乙醇的用途很广,可用乙醇制造醋酸、饮料、香精、染料、燃料等.乙醇的分子结构模型如图所示,下列有关乙醇的说法正确的是( )| A. | 乙醇不属于有机化合物 | |
| B. | 乙醇是由两个碳原子、六个氢原子和一个氧原子构成 | |
| C. | 乙醇的相对分子质量为46g | |
| D. | 乙醇中碳元素的质量分数最大 |
14.燃料电池是一种新型绿色电源,它是将H2、CH4、CO等燃料与空气不断输入,将化学能转化为电能的装置.选择这三种气体作为原料的原因是( )
| A. | 均为无毒无害气体 | B. | 均在大自然中大量存在 | ||
| C. | 均可燃烧生成CO2 | D. | 均可氧化放出大量能量 |


 (1)如图中A仪器的名称是烧杯,燃烧,冷却后打开止水夹,水能进入集气瓶中的原因是:集气瓶中气体减少,压强减小,导致烧杯中的水进入集气瓶.
(1)如图中A仪器的名称是烧杯,燃烧,冷却后打开止水夹,水能进入集气瓶中的原因是:集气瓶中气体减少,压强减小,导致烧杯中的水进入集气瓶.