题目内容
为了探究二氧化碳的性质,某同学设计了如图所示的实验: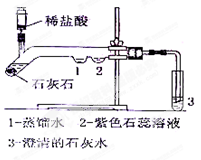
(1)写出石灰石与稀盐酸反应的化学方程式: 。
(2)用注射器注入稀盐酸,一段时间后,可观察到在1、2两处中有一处有明显的现象发生,该实验现象是 。其化学方程式为为 。
(3)3处的澄清石灰水变浑浊,这是由于 的缘故。其化学方程式为 。
(1)2HCl+CaCO3=CaCl2+H2O+CO2↑
(2)第2处紫色石蕊溶液变红 CO2+H2O=H2CO3
(3)生成的碳酸钙不溶于水
Ca(OH) 2+CO2=CaCO3↓+H2O
解析试题分析:(1)石灰石与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:2HCl+CaCO3=CaCl2+H2O+CO2↑
(2)二氧化碳能与水反应生成碳酸,碳酸能使紫色石蕊溶液变红,即2处会变红,反应的化学方程式为: H2O+CO2=H2CO3
(3)生成的二氧化碳会和氢氧化钙反应生成难溶于水的碳酸钙,反应的化学方程式为
Ca(OH) 2+CO2=CaCO3↓+H2O
考点:二氧化碳的性质及二氧化碳的实验室制法

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
除去下列物质中的少量杂质所选用的试剂或方法正确的是
| 选项 | 物质 | 所含杂质 | 所选用试剂或方法 |
| A | NaOH溶液 | Na2CO3溶液 | 稀盐酸 |
| B | CaO | CaCO3 | 高温灼烧 |
| C | CO2 | CO | 点燃 |
| D | 稀盐酸 | 稀硫酸 | 加适量Ba(NO3)2溶液,再过滤 |
实验废液中可能含有离子K+、Mg2+、Cl-、Ba2+、SO42-、CO32-中的几种,为确定可能含有的离子,兴趣小组进行了下面的实验:
①取一份废液,加入氯化钡溶液有白色沉淀产生,再加入足量稀盐酸,沉淀无变化;
②另取一份废液,加入氢氧化钾溶液出现白色沉淀,再加入足量稀盐酸,沉淀全部溶解。
分析上面实验得出的结论中,正确的是
| A.只含有Mg2+、SO42- |
| B.一定含有K+、Mg2+、Cl-、SO42- |
| C.一定含有Mg2+、SO42-,可能含有Cl-、K+ |
| D.一定含有Cl-、K+,可能含有Mg2+、SO42- |