题目内容
钢铁是使用最多的金属材料。下图实验装置是模拟炼铁的实验。其中A是实验室用草酸(H2C2O4)和浓硫酸加热分解产生CO。E是利用得到一氧化碳还原氧化铁得到铁。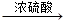
(提示:浓硫酸具有吸水性;草酸分解化学方程式:H2C2O4 H2O+CO2↑+CO↑)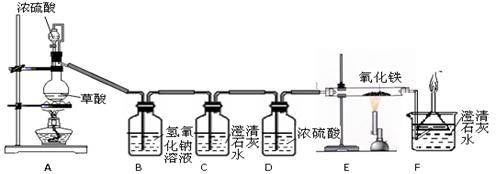
请回答下列问题:
①C装置无明显现象,C装置的作用是 (11) 。
②E装置中的实验现象是 。
③F装置的作用是 。
(11)检验混合气体中二氧化碳是否被除去(12)生成黑色固体(13)检验一氧化碳与氧化铁反应的产物是否含有二氧化碳并尾气吸收
解析

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
(7分)已知某合金样品中可能含有铝、铁、铜中的两种或三种。某小组同学对该合金样品的成分进行探究。
【查阅资料】铝与氢氧化钠溶液可以发生反应,而铁、铜不与氢氧化钠溶液反应。
已知2Al + 2NaOH + 2X= 2NaAlO2 + H2↑,则X的化学式是 。
【探究实验】
| 实验方案 | 实验现象 | 结论 |
| 取一定量的合金样品,加过量的 ,充分反应后过滤,滤渣备用。 取步骤①所得滤渣,加 。 | 样品部分溶解,并有气体放出。 | 合金中一定含有 。 合金中一定含有铁和铜。 |
将Al、Cu分别加入到FeSO4溶液中
将Al、Fe分别加入到CuSO4溶液中
将Al分别加入到FeSO4、CuSO4溶液中
将Fe分别加入到Al2(SO4)3、CuSO4溶液中
实验室可利用碱式碳酸铜(化学式:Cu2(OH)2CO3)制备氧化铜,并进行碳粉还原氧化铜的实验。
①制备氧化铜并检验产物,装置如下图所示(省略夹持仪器):
步骤一:连接A和B,打开活塞,通入空气。
步骤二:关闭活塞,连上C和D,开始加热。
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热。
| 加热时间(min) | 0 | t1 | t2 | t3 |
| B中固体质量(g) | 6.66 | 5.20 | 4.80 | 4.80 |
请在中填入配平后的系数(10)。
C中试剂是(11)。A的作用是吸收空气中的(12),防止对产物检验造成干扰。选择t3时停止加热的理由是(13)。
一定量碳粉还原①中制得的氧化铜并检验产物,装置如下图所示:
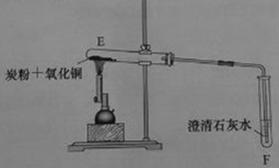
实验过程中,观察到F中溶液变浑浊,E中的现象是(14)。
反应完全后,若仅撤走酒精喷灯停止加热,可能导致的后果是(15)。
分析:若①中省略步骤三,对②中反应产物判断可能产生的影响及其原因。
(16)
下列有关物质鉴别方案正确的一组是:
| A.可用Ba(OH)2溶液鉴别(NH4)2CO3、(NH4)2SO4、NH4NO3三种氮肥 |
| B.MgCl2溶液、NaOH溶液、H2SO4溶液、CuSO4溶液,不加任何试剂即可鉴别 |
| C.Na2CO3溶液、Ca(OH)2溶液、盐酸、BaCl2溶液,不加任何试剂即可鉴别 |
| D.CuO粉末、炭粉、铁粉,三种黑色粉末用一种试剂无法鉴别 |