题目内容
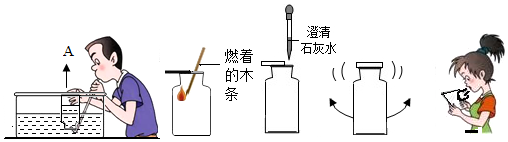
11.人教版新化学教材关于“分解过氧化氢制氧气的反应中二氧化锰的催化作用“以及”寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣.【实验探究】
| 实验步骤 | 实验现象 |
| Ⅰ.分别量取5mL5%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁( Fe2O3)粉末,并分别在A、B两支试管中插入带火星木条,观察现象. | A试管中产生气泡,带火星木条复燃,B试管中无明显现象. |
| Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次实验,观察现象. | 试管中均产生气泡,带火星木条均复燃. |
| Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得虑渣进行洗涤、干燥、称量,所得固体质量仍为a克. | / |
| Ⅳ.在装有a克氧化铁粉末的C试管、装有a克二氧化锰粉末的D中分别放入5mL5%过氧化氢溶液,观察现象. | / |
【实验结论】实验Ⅱ、Ⅲ证明:氧化铁(Fe2O3)的质量和化学性质在反应前后均没有发生变化,可以作过氧化氢分解的催化剂.
写出氧化铁(Fe2O3)催化过氧化氢分解的化学符号表达式2H2O2$\frac{\underline{\;三氧化二铁\;}}{\;}$2H2O+O2↑.
【实验评价】设计实验Ⅳ的目的是探究氧化铁的催化效果是否比二氧化锰的更好.
若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是二氧化锰更适合做过氧化氢分解生成氧气的催化剂.
【实验拓展】
查阅资料得知:CuO、CuSO4、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂.下列有关催化剂的说法中正确的是B(填序号).
A.MnO2只能作为过氧化氢溶液分解的催化剂
B.同一个化学反应可以有多种催化剂
C.催化剂只能加快化学反应的速率
D.用作催化剂的物质不可能是其它反应的反应物或生成物.
若答对下列问题将奖励4分,但化学试卷总分不超过60分.为探究“二氧化锰的质量对过氧化氢分解反应速率的影响”,小组同学在老师的指导下又进行了如下实验:
Ⅰ.按图甲组装实验仪器并进行气密性检测
Ⅱ.取10毫升溶质质量分数为3%的过氧化氢溶液和0.03克二氧化锰装入容器,塞紧橡皮塞,接上压强测量仪(如图乙)
Ⅲ.倾斜装置,使过氧化氢溶液和二氧化锰充分混合,用压强测量仪测量容器内的气压
Ⅳ.分别用0.06克、0.09克和0.12克相同的二氧化锰重复上述实验,整理相关数据如图丙.
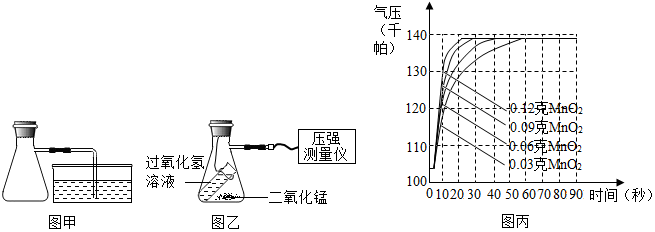
①写出步骤Ⅰ中检查装置气密性的具体操作及气密性良好的判断依据:用手捂住锥形瓶,导管口出现气泡,说明装置不漏气.
②实验中,小组同学用容器内压强的大小来反映产生氧气的多少.
③该探究过程得出的结论是二氧化锰的质量对反应速率的影响.
分析 【实验结论】(1)根据氧气具有助燃性,能使带火星木条复燃进行解答;
(2)根据实验Ⅱ、Ⅲ证明:氧化铁的质量和化学性质在反应前后均没有发生变化,可以作过氧化氢分解的催化剂进行解答;
(3)根据氧化铁催化过氧化氢分解生成水和氧气进行解答;
【实验评价】根据若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是二氧化锰更适合做过氧化氢分解生成氧气的催化剂进行解答;
【实验拓展】根据催化剂的含义进行解答.
凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
容器内压强越大,说明产生的氧气越多;
根据图中数据可以判断相关方面的问题.
解答 解:【实验结论】(1)氧气具有助燃性,能使带火星木条复燃,所以有实验现象A试管中产生气泡,带火星木条复燃,可知A中产生的气体是氧气;硫在氧气中燃烧发出明亮的蓝紫色火焰,过滤过程中玻璃棒的作用是引流;
(2)实验Ⅱ、Ⅲ证明:氧化铁的质量和化学性质在反应前后均没有发生变化,可以作过氧化氢分解的催化剂;故填:质量;化学性质;
(3)氧化铁催化过氧化氢分解生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;三氧化二铁\;}}{\;}$2H2O+O2↑;
【实验评价】若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是二氧化锰更适合做过氧化氢分解生成氧气的催化剂;故填:二氧化锰更适合做过氧化氢分解生成氧气的催化剂;
【实验拓展】A.MnO2不只能作为氧化氢溶液分解的催化剂,还可以作其他反应的催化剂,故A错误;
B.根据题目的信息可知同一个化学反应可以有多种催化剂,故B正确;
C.催化剂不只是加快化学反应的速率,还能减慢化学反应的速率,故C错误;
D.用作催化剂的物质可能是其它反应的反应物或生成物,例如二氧化锰是高锰酸钾受热分解制氧气的生成物,故D错误;
①步骤Ⅰ中检查装置气密性的具体操作及气密性良好的判断依据是:用手捂住锥形瓶,导管口出现气泡,说明装置不漏气.
②实验中,容器内气体的压强越大,说明产生的氧气越多,压强越小,说明产生的氧气越少,因此小明是用容器内压强的大小来反映产生氧气的多少.
③由图中数据可知,二氧化锰的质量大小能够影响反应的速率,但是不影响产生氧气的质量,因此本实验除了研究“二氧化锰质量对过氧化氢分解产生氧气质量的影响外”还可以研究的问题是二氧化锰的质量对反应速率的影响.
故答案为:【实验结论】(1)蓝紫;引流;(2)质量;化学性质;(3)2H2O2$\frac{\underline{\;三氧化二铁\;}}{\;}$2H2O+O2↑;【实验评价】二氧化锰更适合做过氧化氢分解生成氧气的催化剂;【实验拓展】B.①用手捂住锥形瓶,导管口出现气泡,说明装置不漏气.
②容器内压强的大小.
③二氧化锰的质量对反应速率的影响.
点评 此题考查了催化剂的特点与催化作用,以及实验室中制取氧气的反应原理来解答此题,锻炼了学生分析问题解决问题能力.

 阅读快车系列答案
阅读快车系列答案【提出问题】哪些因素可能影响该反应的反应速率?
【查阅资料】影响化学反应速率的因素:
①主要因素:反应物本身的性质;
②外界因素:温度,浓度,压强,催化剂,光,激光,反应物颗粒大小,反应物之间的接触面积和反应物状态;
③另外,x射线,γ射线也会影响化学反应速率.
【作出猜想】下面是小组内三位同学所做的猜想,请你完成小丽的猜想.
小红同学:H2O2溶液的浓度可能影响该反应的反应速率.
小明同学:催化剂(MnO2)的用量可能影响该反应的反应速率.
小丽同学:我认为(1)温度可能影响该反应的反应速率.
【实验验证】
(2)小红同学的实验是:每次均取10mL30%的H2O2溶液,然后稀释成不同浓度的溶液进行实验,测定各次收集到100mL氧气时所用的时间,记录数据如表:(其他实验条件:温度、催化剂用量等均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 |
| H2O2溶液浓度 | 1% | 5% | 15% | 25% | 30% |
| 所用时间(秒) | 660 | 205 | 25 | 4 | 3 |
(3)小明同学的实验是:每次均用30mL10%的H2O2溶液,采用不同量MnO2粉末做催化剂,测定各次收集到500mL氧气时所用的时间,结果如表:(其他实验条件:过氧化氢溶液浓度、温度等均相同)
请你分析回答:该反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
| 实验次序 | 1 | 2 | 3 | 4 | 5 |
| MnO2 粉末用量(克) | 0.2 | 0.4 | 0.6 | 0.8 | 1.0 |
| 所用时间(秒) | 8 | 5 | 3 | 2 | 2 |
(4).如果你是小丽同学,在验证你的猜想时,你的实验方案是:分别在20℃、40℃条件下,向等浓度、等体积的过氧化氢溶液中,加入等质量的二氧化锰粉末,测量各收集一瓶等体积氧气所需要的时间
每次均用30mL10%的H2O2溶液,采用不同温度,测定各次收集到500mL氧气时所用的时间,结果如表:(过氧化氢质量分数、催化剂等均相同)
| 实验次序 | 1 | 2 | 3 |
| 过氧化氢的质量分数 | 10% | 10% | 10% |
| 反应温度控制(℃) | 10 | 30 | 50 |
| MnO2 粉末用量(克) | 0.2 | 0.2 | 0.2 |
| 所用时间(秒) |
| A. | 一个分子中含有11个氢分子 | B. | 一个分子中含有42个原子 | ||
| C. | 青蒿素中碳、氧元素的质量比为9:4 | D. | 青蒿素中氧元素的质量分数最小 |
 将二氧化碳气体缓缓通入质量分数为0.2的氢氧化钠溶液中,溶液中某元素质量分数y随时间的变化趋势如图.则y坐标表示的是( )
将二氧化碳气体缓缓通入质量分数为0.2的氢氧化钠溶液中,溶液中某元素质量分数y随时间的变化趋势如图.则y坐标表示的是( )| A. | 钠元素的质量分数 | B. | 氧元素的质量分数 | ||
| C. | 氢元素的质量分数 | D. | 碳元素的质量分数 |