题目内容
1. 将二氧化碳气体缓缓通入质量分数为0.2的氢氧化钠溶液中,溶液中某元素质量分数y随时间的变化趋势如图.则y坐标表示的是( )
将二氧化碳气体缓缓通入质量分数为0.2的氢氧化钠溶液中,溶液中某元素质量分数y随时间的变化趋势如图.则y坐标表示的是( )| A. | 钠元素的质量分数 | B. | 氧元素的质量分数 | ||
| C. | 氢元素的质量分数 | D. | 碳元素的质量分数 |
分析 根据反应的化学方程式和图中通过的数据可以判断相关方面的问题.
解答 解:A、随着反应的进行,溶液中钠元素的质量不变,该选项说法不正确;
B、随着反应的进行,溶液中开始就有氧元素,所以氧元素的质量分数不是从0开始增长的,最后氢氧化钠溶液反应完,氧元素的质量分数不再变化,故该选项说法不正确;
C、随着反应的进行,氢元素的质量分数不变,该选项说法不正确;
D、随着反应的进行,二氧化碳不断反应形成溶液的一部分,因此溶液中碳元素的质量不断增大,当恰好完全反应时,质量不再增大,该选项说法正确.
故选:D
点评 本题主要考查物质的性质,只有掌握了各种物质的性质,才能够判断物质之间相互转化时的反应物和生成物,从而可以进行各方面的判断.

练习册系列答案
相关题目
11.人教版新化学教材关于“分解过氧化氢制氧气的反应中二氧化锰的催化作用“以及”寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣.
【实验探究】
实验Ⅰ的A试管中若伸入燃烧的硫,则产生明亮的蓝紫色火焰,实验Ⅲ中“将实验Ⅱ中的剩余物小心过滤”时使用的玻璃棒,其作用是引流.
【实验结论】实验Ⅱ、Ⅲ证明:氧化铁(Fe2O3)的质量和化学性质在反应前后均没有发生变化,可以作过氧化氢分解的催化剂.
写出氧化铁(Fe2O3)催化过氧化氢分解的化学符号表达式2H2O2$\frac{\underline{\;三氧化二铁\;}}{\;}$2H2O+O2↑.
【实验评价】设计实验Ⅳ的目的是探究氧化铁的催化效果是否比二氧化锰的更好.
若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是二氧化锰更适合做过氧化氢分解生成氧气的催化剂.
【实验拓展】
查阅资料得知:CuO、CuSO4、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂.下列有关催化剂的说法中正确的是B(填序号).
A.MnO2只能作为过氧化氢溶液分解的催化剂
B.同一个化学反应可以有多种催化剂
C.催化剂只能加快化学反应的速率
D.用作催化剂的物质不可能是其它反应的反应物或生成物.
若答对下列问题将奖励4分,但化学试卷总分不超过60分.为探究“二氧化锰的质量对过氧化氢分解反应速率的影响”,小组同学在老师的指导下又进行了如下实验:
Ⅰ.按图甲组装实验仪器并进行气密性检测
Ⅱ.取10毫升溶质质量分数为3%的过氧化氢溶液和0.03克二氧化锰装入容器,塞紧橡皮塞,接上压强测量仪(如图乙)
Ⅲ.倾斜装置,使过氧化氢溶液和二氧化锰充分混合,用压强测量仪测量容器内的气压
Ⅳ.分别用0.06克、0.09克和0.12克相同的二氧化锰重复上述实验,整理相关数据如图丙.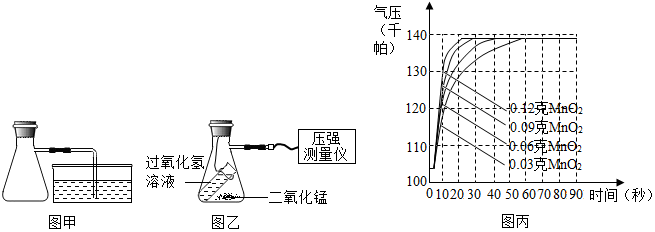
①写出步骤Ⅰ中检查装置气密性的具体操作及气密性良好的判断依据:用手捂住锥形瓶,导管口出现气泡,说明装置不漏气.
②实验中,小组同学用容器内压强的大小来反映产生氧气的多少.
③该探究过程得出的结论是二氧化锰的质量对反应速率的影响.
【实验探究】
| 实验步骤 | 实验现象 |
| Ⅰ.分别量取5mL5%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁( Fe2O3)粉末,并分别在A、B两支试管中插入带火星木条,观察现象. | A试管中产生气泡,带火星木条复燃,B试管中无明显现象. |
| Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次实验,观察现象. | 试管中均产生气泡,带火星木条均复燃. |
| Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得虑渣进行洗涤、干燥、称量,所得固体质量仍为a克. | / |
| Ⅳ.在装有a克氧化铁粉末的C试管、装有a克二氧化锰粉末的D中分别放入5mL5%过氧化氢溶液,观察现象. | / |
【实验结论】实验Ⅱ、Ⅲ证明:氧化铁(Fe2O3)的质量和化学性质在反应前后均没有发生变化,可以作过氧化氢分解的催化剂.
写出氧化铁(Fe2O3)催化过氧化氢分解的化学符号表达式2H2O2$\frac{\underline{\;三氧化二铁\;}}{\;}$2H2O+O2↑.
【实验评价】设计实验Ⅳ的目的是探究氧化铁的催化效果是否比二氧化锰的更好.
若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是二氧化锰更适合做过氧化氢分解生成氧气的催化剂.
【实验拓展】
查阅资料得知:CuO、CuSO4、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂.下列有关催化剂的说法中正确的是B(填序号).
A.MnO2只能作为过氧化氢溶液分解的催化剂
B.同一个化学反应可以有多种催化剂
C.催化剂只能加快化学反应的速率
D.用作催化剂的物质不可能是其它反应的反应物或生成物.
若答对下列问题将奖励4分,但化学试卷总分不超过60分.为探究“二氧化锰的质量对过氧化氢分解反应速率的影响”,小组同学在老师的指导下又进行了如下实验:
Ⅰ.按图甲组装实验仪器并进行气密性检测
Ⅱ.取10毫升溶质质量分数为3%的过氧化氢溶液和0.03克二氧化锰装入容器,塞紧橡皮塞,接上压强测量仪(如图乙)
Ⅲ.倾斜装置,使过氧化氢溶液和二氧化锰充分混合,用压强测量仪测量容器内的气压
Ⅳ.分别用0.06克、0.09克和0.12克相同的二氧化锰重复上述实验,整理相关数据如图丙.

①写出步骤Ⅰ中检查装置气密性的具体操作及气密性良好的判断依据:用手捂住锥形瓶,导管口出现气泡,说明装置不漏气.
②实验中,小组同学用容器内压强的大小来反映产生氧气的多少.
③该探究过程得出的结论是二氧化锰的质量对反应速率的影响.
12.中国女药学家屠呦呦因发现抗疟新药青蒿素(化学式C15H22O5)而获得诺贝尔医学或生理学奖.青蒿素是白色针状结晶,味苦,几乎不溶于水.下列有关青萵素的说法正确的是( )
| A. | “味苦,几乎不溶于水”属于青蒿素的化学性质 | |
| B. | 青蒿素不属于氧化物 | |
| C. | 青蒿素中碳、氢和氧三种元素质量比是15:22:5 | |
| D. | 青蒿素由15个碳原子、22个氢原子和5个氧原子构成 |
9.天气预报时,下列指标不会预报的是( )
| A. | PM2.5 | B. | 二氧化硫浓度 | C. | 氮氧化合物浓度 | D. | 二氧化碳浓度 |
16.下列实验现象描述错误的是( )
| A. | 硫在氧气中燃烧,火焰呈蓝紫色 | |
| B. | 氢氧化钠溶液中滴加硫酸铜溶液,生成蓝色絮状硫酸铜沉淀 | |
| C. | 在大理石上滴加稀盐酸,有气泡生成 | |
| D. | 镁带在空气中燃烧,发出耀眼白光,生成白色粉末 |
4.对石蜡燃烧时的现象,下列描述正确的是( )
| A. | 石蜡硬度小,不溶于水 | |
| B. | 蜡烛密度比水小,浮在水面上 | |
| C. | 可以观察到石蜡燃烧时产生水和二氧化碳 | |
| D. | 石蜡在空气中燃烧时有明亮火焰,稍有黑烟产生 |
 下列各物质均是常见的单质或化合物,它们之间有如图所示的转化关系.已知:B、H是红色粉末,A、E、M是黑色粉末,C和F是含有相同元素的气体,G的溶液显浅绿色,①③④处均发生的是置换反应.
下列各物质均是常见的单质或化合物,它们之间有如图所示的转化关系.已知:B、H是红色粉末,A、E、M是黑色粉末,C和F是含有相同元素的气体,G的溶液显浅绿色,①③④处均发生的是置换反应. 如图是铁丝在氧气中燃烧实验的操作图.试回答下列问题:
如图是铁丝在氧气中燃烧实验的操作图.试回答下列问题: