题目内容
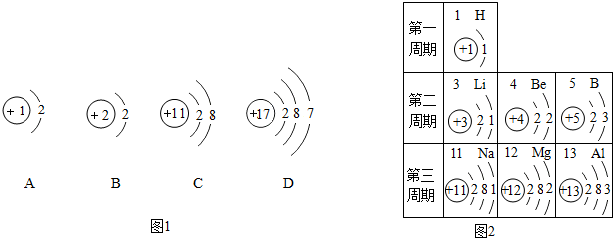
17. 如图是某种粒子(原子或离子)的结构示意图
如图是某种粒子(原子或离子)的结构示意图(1)若m=11,则该粒子所对应元素的符号为Na.
(2)若该粒子带两个单位负电荷,且n=8,则该粒子的符号为S2-.
(3)若m-n<10,则该粒子是一个阴离子(选填“原子”“阳离子”或“阴离子”).
分析 (1)由粒子(原子或离子)的结构示意图为 和m=11可知,n的值,则可知元素符号;
和m=11可知,n的值,则可知元素符号;
(2)由已知条件该粒子带两个单位负电荷,且n=8,可知m的值,则可知粒子符号;
(3)若m-n<10,说明得电子了,故可知其离子种类.
解答 解:(1)由粒子(原子或离子)的结构示意图为 和m=11可知,n的值为1,则可知元素符号为Na;
和m=11可知,n的值为1,则可知元素符号为Na;
(2)由已知条件该粒子带两个单位负电荷,且n=8,则知原子得2个电子,可知m的值为(2+8+8)-2=16,为硫元素,则可知粒子符号为S2-;
(3)若m-n<10,说明得电子了,故可知其离子种类为阴离子.(可以举具体数字代入验证.)
故答为:(1)Na;(2)S2-;(3)阴离子.
点评 了解原子和离子的相互转化;掌握原子结构示意图与离子结构示意图的区别、特点;掌握元素的符号及其意义.

练习册系列答案
相关题目
7.(1)现有下列试剂:硫酸铜溶液、硝酸银溶液、硫酸铝溶液、铜片、铝片.某校九年级1班化学兴趣小组设计了下列实验方案,请你和他们一起探究银、铝、铜三种金属的活动性强弱.
(2)①化学知识跟日常生活关系非常密切,用化学方程式解释下列问题:
新鲜鸡蛋呼吸时会放出二氧化碳,可把鸡蛋放在石灰水中保鲜.化学方程式:Ca(OH)2+CO2=CaCO3↓+H2O.
②用稀硫酸清洗铁制品表面的铁锈(主要成分Fe2O3).化学方程式:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O.
| 实验步骤 | 实验现象 | 实验结论 |
| 把铝片打磨后,放入装有a:硫酸铜溶液烧杯中,观察 | 铝片表面覆盖一层b:红色的铜 | 三种金属的活动性由强到弱的顺序为: e:铝、铜、银 |
| 把铜片打磨后,放入装有c:硝酸银溶液烧杯中,观察 | 铜片表面覆盖一层d:银白色的银 |
新鲜鸡蛋呼吸时会放出二氧化碳,可把鸡蛋放在石灰水中保鲜.化学方程式:Ca(OH)2+CO2=CaCO3↓+H2O.
②用稀硫酸清洗铁制品表面的铁锈(主要成分Fe2O3).化学方程式:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O.
5.科学家利用高温高压技术成功合成出超高硬度的纳米孪晶结构立方氮化硼块材,氮化硼中氮和硼的化合价分别为-3价和+3价.则氮化硼的化学式为( )
| A. | NB | B. | BN | C. | bN | D. | B3N3 |
12.下列不属于化合反应,也不属于分解反应,但属于氧化反应的是( )
| A. | 木炭+氧气$\stackrel{点燃}{→}$二氧化碳 | B. | 石蜡+氧气$\stackrel{点燃}{→}$水+二氧化碳 | ||
| C. | 铝+氧气$\stackrel{点燃}{→}$氧化铝 | D. | 氧化汞$\stackrel{加热}{→}$汞+氧气 |
2.实现“低碳经济”的一种策略是节约能源.下列制备氢气的方法最节能的是( )
| A. | 电解水:2H2O $\frac{\underline{\;通电\;}}{\;}$ 2H2↑+O2↑ | |
| B. | 焦炭与水蒸气反应:C+H2O$\frac{\underline{\;高温\;}}{\;}$H2+CO | |
| C. | 太阳光分解水:2H2O$\frac{\underline{\;\;\;TiO_{2}\;\;\;}}{太阳光}$2H2↑+O2↑ | |
| D. | 天然气与水蒸气反应:CH4+H2O $\frac{\underline{\;高温\;}}{\;}$ CO+3H2 |