题目内容
12.实验室制取某些气体所用的装置如图1所示,请回答:
(1)图中标号a的仪器名称是长颈漏斗.
(2)实验室用高锰酸钾制取氧气,反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.若用D装置收集氧气,气体应从b(填“b”或“c”)端进入.
(3)乙炔(C2H2)是一种可燃性气体,己知实验室可用块状电石和水在常温下反应制取,该反应非常剧烈,则制取乙炔气体的发生装置最好选择C(填字母).如果要得到干燥的乙炔气体,可以在D装置中加入浓硫酸,收集乙炔的集气瓶应与D装置的c(填“b”或“c”)端连接.
(4)用氯酸钾和二氧化锰制备氧气时,二氧化锰在反.应中的作用是催化作用.利用如图2所示流程分离并回收充分反应后的剩余固体,请回答下列问题. (二氧化锰不溶于水)操作m的名称是过滤.操作m和操作n中都用到的玻璃仪器是玻璃棒,操作m中该 仪器的作用是引流.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,氧气的密度比空气大进行分析;
(3)根据分液漏斗可以控制液体的滴加速度,浓硫酸有吸水性,洗气应该长进短出,乙炔密度比空气小进行分析;
(4)根据二氧化锰是氯酸钾分解的催化剂,过滤可以将不溶性固体从溶液中分离出来,玻璃棒在过滤操作中的作用是引流进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,a是长颈漏斗;
(2)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,氧气的密度比空气大,所以用D装置收集氧气,气体应从b端进入;
(3)分液漏斗可以控制液体的滴加速度,所以制取乙炔气体的发生装置最好选择C,浓硫酸有吸水性,洗气应该长进短出,所以要得到干燥的乙炔气体,可以在D装置中加入浓硫酸,乙炔密度比空气小,所以收集乙炔的集气瓶应与D装置的c端连接;
(4)二氧化锰是氯酸钾分解的催化剂,起催化作用,过滤可以将不溶性固体从溶液中分离出来,在过滤、蒸发的操作过程中都会用到玻璃棒,玻璃棒在过滤操作中的作用是引流.
故答案为:(1)长颈漏斗;
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,b;
(3)C,浓硫酸,乙炔密度比空气小,c;
(4)催化作用,过滤,玻璃棒,引流.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
7.下列实验操作中,错误的是( )
| A. |  加粉末状固体 | B. |  观察读数 | C. |  用胶头滴管滴液 | D. |  加热液体 |
8.下列物质的转变,不能一步实现的是( )
| A. | Fe(NO3)2→AgNO3 | B. | SO3→Na2SO4 | C. | KCl→KNO3 | D. | H2→Cu |
5.下列实验操作错误的是.
| A. | 木炭放入燃烧匙中加热到发红,然后迅速伸入到氧气瓶底部 | |
| B. | 硫在氧气中燃烧实验所用的燃烧匙内应预先垫上一层石棉布 | |
| C. | 铁丝在氧气中燃烧时,应先将洁净的细铁丝绕成螺旋状 | |
| D. | 细铁丝燃烧的氧气瓶中应先装有少量的水或细沙 |
1.医学上治疗中重度妊娠高血压症需要用到25%的硫酸镁注射液,下表是硫酸镁的部分溶解度数据:
若用无水硫酸镁固体配制10 克25%的硫酸镁溶液,如图为溶液配制过程,
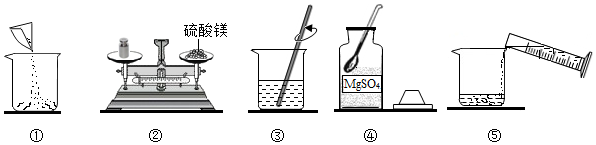
(1)请指出图②中操作错误之处砝码与药品位置放反了
(2)用如图所示的序号表示正确配制该溶液的操作顺序为④②①⑤③
(3)医学人士认为,该注射液在10℃以下不宜使用,请结合上表说明理由:10℃以下时,硫酸镁饱和溶液中溶质质量分数小于25%.
| 温度(℃) | 10 | 20 | 30 | 40 | 60 | 80 |
| 溶解度(g/100g水) | 28.2 | 33.7 | 38.9 | 44.5 | 54.6 | 55.8 |

(1)请指出图②中操作错误之处砝码与药品位置放反了
(2)用如图所示的序号表示正确配制该溶液的操作顺序为④②①⑤③
(3)医学人士认为,该注射液在10℃以下不宜使用,请结合上表说明理由:10℃以下时,硫酸镁饱和溶液中溶质质量分数小于25%.


