题目内容
17.在国民经济中,生产化学产品的工业,统称为化学工业.下列产品,主要不是应用化学反应进行生产的是( )| A. | 水泥、钢材 | B. | 化肥、农药 | ||
| C. | 侯氏制碱法制纯碱 | D. | 海水晒盐 |
分析 根据已有的知识进行分析解答,通过化学反应进行生产则是发生化学变化,据此解答.
解答 解:A、水泥和钢材是通过发生化学反应生成的;
B、化肥和农药是通过化学反应生成的;
C、纯碱是通过化学反应生成的;
D、海水晒盐是物理变化;
故选D.
点评 本题考查的是物理变化和化学变化的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
8.下列有关化学符号“H2O”表示的意义,错误的是( )
| A. | 水这种物质 | |
| B. | 一个水分子由两个氢原子和一个氧原子构成 | |
| C. | 一个水分子中含有一个氢分子 | |
| D. | 水由氢元素和氧元素组成 |
12.铝合金是工业中应用最广泛的一类有色金属结构材料,在航空、航天、汽车、机械制造、船舶及化学工业中已大量应用.工业经济的飞速发展,对铝合金的需求日益增多,使铝合金的研究也随之深入.已知某合金粉末除铝外,还含有铁、铜中的一种或两种.某兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究.
查阅资料:铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应.
猜想1:该合金粉末中除铝外,还含有铁.
猜想2:该合金粉末中除铝外,还含有铜(填名称).
猜想3:该合金粉末中除铝外,还含有铁、铜.
实验探究:下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液.
探究结论:猜想3成立.
反思:一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.写出铝与稀盐酸反应的化学方程式2Al+6HCl═2AlCl3+3H2↑.
查阅资料:铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应.
猜想1:该合金粉末中除铝外,还含有铁.
猜想2:该合金粉末中除铝外,还含有铜(填名称).
猜想3:该合金粉末中除铝外,还含有铁、铜.
实验探究:下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液.
| 实验方案 | 实现现象 | 结论 |
| ①取一定量的合金粉末,加过量的30% NaOH溶液,充分反应后过滤,滤渣备用. | 粉末部分溶解,并有气体放出. | 合金中一定含有铝. |
| ②取步骤①所得滤渣,加过量的10% 盐酸,充分反应. | 滤渣部分溶解,并有气体放出,溶液呈浅绿色. | 合金中一定含有铁和铜. |
反思:一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.写出铝与稀盐酸反应的化学方程式2Al+6HCl═2AlCl3+3H2↑.
2.实验室用高锰酸钾制取氧气的实验中,不需要用到的一组仪器是( )
| A. | 烧杯、玻璃棒 | B. | 大试管、集气瓶 | C. | 导管、单孔塞 | D. | 酒精灯、铁架台 |
6.在如图所示的维恩图中,①、②、③、④可分别代表( )

| A. | 金属元素、非金属元素、放射性元素、所有元素 | |
| B. | 氧气、氮气、其他成分、空气 | |
| C. | 单质、化合物、氧化物、纯净物 | |
| D. | 单质、混合物、化合物、所有物质 |
7.取一定质量Fe2O3与Al2O3的混合物,恰好和100g质量分数为9.8%稀硫酸完全反应,原混合物中氧元素的质量是( )
| A. | 0.8g | B. | 1.6g | C. | 1.8g | D. | 3.6g |
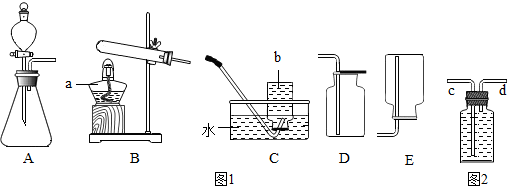
 甲、乙两个装置均可用于证明SO2易溶于水.
甲、乙两个装置均可用于证明SO2易溶于水.