题目内容
3.向一定质量的氧化铜和氢氧化铜的固体混合物中加入91g的稀硫酸,恰好完全反应,形成100g溶液,则所得溶液中溶质的质量分数最有可能是( )| A. | 8% | B. | 16% | C. | 24% | D. | 32% |
分析 根据氧化铜和硫酸反应生成硫酸铜和水,氢氧化铜和硫酸铜反应生成硫酸铜和水,可以假设增加的9g全部是氧化铜或氢氧化铜,然后依据化学方程式进行计算.
解答 解:假设9g全部是氧化铜,设生成硫酸铜质量为x
CuO------CuSO4,
80 160
9g x
$\frac{80}{9g}$=$\frac{160}{x}$
x=18g
所得溶液中溶质的质量分数为18%,
假设9g全部是氢氧化铜,设生成硫酸铜质量为y
Cu(OH)2-----CuSO4,
98 160
9g y
$\frac{80}{9g}$=$\frac{160}{y}$
y=14.5g
所得溶液中溶质的质量分数为14.5%,
但是固体是氧化铜和氢氧化铜的混合物,所以所得溶液中溶质的质量分数最有可能是在14.5%和18%之间,故选:B.
点评 本题主要考查了化学方程式的计算,难度不大,注意极端法在化学方程式计算中的应用.

练习册系列答案
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
14.非诺洛芬是一种治疗类风湿关节炎的药物,化学式为C15H14O3,以下不正确的是( )
| A. | 该药物由三种元素组成 | B. | 一个非诺洛芬分子有32个原子 | ||
| C. | 该药物相对分子质量为242 | D. | 碳氢氧三种元素质量比为15:14:3 |
11.某白色固体A可能含有碳酸钠、氯化钡(水溶液呈中性)、氢氧化钠中的一种或几种,进行如下实验:
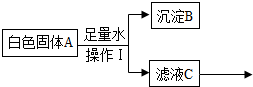
完成下列填空:
①根据上述实验分析,A中一定含有的物质是碳酸钠、氯化钡,写出生成B的化学方程式:Na2CO3+BaCl2═BaCO3↓+2NaCl.
②为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成如表.

完成下列填空:
①根据上述实验分析,A中一定含有的物质是碳酸钠、氯化钡,写出生成B的化学方程式:Na2CO3+BaCl2═BaCO3↓+2NaCl.
②为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成如表.
| 实验操作 | 现象 | 结论 |
| 向滤液C中加入足量的氯化钡溶液,充分反应后,静置,取上层清液滴加无色酚酞 | 无色酚酞变红色 | A中有氢氧化钠 |
8.下列各组离子可在同一溶液中大量共存的是( )
| A. | H+ SO42- K+ CO32- | B. | Mg2+ Cl- OH- Na+ | ||
| C. | Fe3+ SO42- H+ Cl- | D. | Na+ Ba2+ NO3- SO42- |
15.化学改变世界的途径是使物质发生化学变化.下列变化属于化学变化的是( )
| A. |  树根“变”根雕 | B. |  葡萄“变”美酒 | ||
| C. |  玉石“变”印章 | D. |  玩具机器人“变”形 |
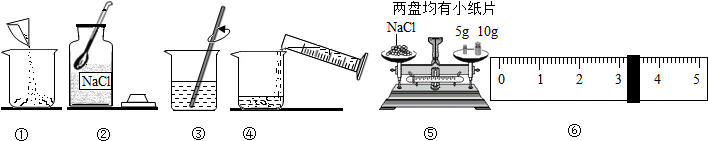 (1)用图中序号表示配制溶液的正确操作顺序②⑤①④③.
(1)用图中序号表示配制溶液的正确操作顺序②⑤①④③. 材料的应用,极大地促进了人类社会的发展和人们生活水平的提高,请从化学视角回答下列问题:
材料的应用,极大地促进了人类社会的发展和人们生活水平的提高,请从化学视角回答下列问题: