题目内容
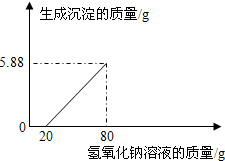 某化学小组要测定氧化铜样品(含杂质不溶于水,也不与盐酸反应)中氧化铜的含量,现取该样品5g与足量的稀盐酸反应,过滤得到滤液100g,再向滤液中加入氢氧化钠溶液,反应的实验数据如图所示.请计算:
某化学小组要测定氧化铜样品(含杂质不溶于水,也不与盐酸反应)中氧化铜的含量,现取该样品5g与足量的稀盐酸反应,过滤得到滤液100g,再向滤液中加入氢氧化钠溶液,反应的实验数据如图所示.请计算:(1)该样品中氧化铜的质量分数为
96%
96%
.(2)所加氢氧化钠溶液中溶质的质量分数为多少?
分析:(1)根据物质间的反应:氧化铜与盐酸反应生成了氯化铜和水,氯化铜与氢氧化钠反应生成了氯化钠和氢氧化铜沉淀.找出氧化铜与生成的氢氧化铜的质量关系式,由氢氧化铜的质量可求出氧化铜的质量,再求出样品中氧化铜的质量分数;
(2)根据实验数据图分析,由氢氧化铜的质量可求出与氯化铜反应生的氢氧化钠溶液中溶质的质量,再求出所加氢氧化钠溶液中溶质的质量分数.
(2)根据实验数据图分析,由氢氧化铜的质量可求出与氯化铜反应生的氢氧化钠溶液中溶质的质量,再求出所加氢氧化钠溶液中溶质的质量分数.
解答:解:(1)设氧化铜的质量为X
由题可知:CuO+2HCl=CuCl2+H2O,2NaOH+CuCl2=Cu(OH)2↓+2NaCl
可得出:CuO~Cu(OH)2
80 98
x 5.88g
=
解得:x=4.8g
该样品中氧化铜的质量分数为:
×100%=96%
(2)由实验数据图可知,与氯化铜反应生成5.88g沉淀所需的氢氧化钠溶液质量为:80g-20g=60g.
设60g氢氧化钠溶液中含氢氧化钠质量为y
2NaOH+CuCl2=Cu(OH)2↓+2NaCl
80 98
y 5.88g
=
解得:y=4.8g
所加氢氧化钠溶液中溶质的质量分数为:
×100%=8%.
故答为:(1)96%;(2)所加氢氧化钠溶液中溶质的质量分数为8%
由题可知:CuO+2HCl=CuCl2+H2O,2NaOH+CuCl2=Cu(OH)2↓+2NaCl
可得出:CuO~Cu(OH)2
80 98
x 5.88g
| 80 |
| 98 |
| x |
| 5.88g |
该样品中氧化铜的质量分数为:
| 4.8g |
| 5g |
(2)由实验数据图可知,与氯化铜反应生成5.88g沉淀所需的氢氧化钠溶液质量为:80g-20g=60g.
设60g氢氧化钠溶液中含氢氧化钠质量为y
2NaOH+CuCl2=Cu(OH)2↓+2NaCl
80 98
y 5.88g
| 80 |
| 98 |
| y |
| 5.88g |
所加氢氧化钠溶液中溶质的质量分数为:
| 4.8g |
| 60g |
故答为:(1)96%;(2)所加氢氧化钠溶液中溶质的质量分数为8%
点评:本题在解题时,利用物质间反应的方程式,找出物质间的关系式,利用关系式进行计算较为简便.

练习册系列答案
相关题目