题目内容
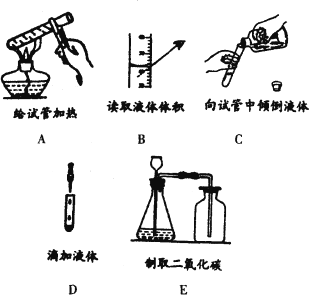
(1)化学实验基本操作在化学学习和探究中具有重要作用.正确的操作是实验成功的重要保证,说出各操作的理由.
①熄灭酒精灯时,应盖灭后轻提一下灯帽,再重新盖好
②粗盐提纯实验中之蒸发时,要用玻璃棒不断搅拌
(2)理解与应用
①为了验证Zn、Fe、Cu三种金属活动顺序为:Zn>Fe>Cu这一结论,下面实验设计不合理的是
A.将Zn、Cu分别放入FeSO4溶液中
B.将相同条件下的Zn、Fe、Cu分别放入稀硫酸溶液中
C.将Fe分别放入ZnSO4、CuSO4溶液中
D.将Zn、Cu分别放入CuSO4溶液中
②甲化工厂排出的废水中含有少量氢氧化钾和硫酸钾,某实验小组对乙化工厂排出的废水测定后,决定将甲、乙两化工厂的废水按一定比例混合,所得溶液pH=7,且只含有氯化钾一种溶质溶液用作农田灌溉.乙化工厂的废水中含有的物质是(填化学式)
①熄灭酒精灯时,应盖灭后轻提一下灯帽,再重新盖好
第一次盖灭火焰但灯帽内存有热的空气,如果不再盖第二次的话灯帽内热的空气冷却后压强减小,在外界大气压的作用下,下次再用时不容易拔下来
第一次盖灭火焰但灯帽内存有热的空气,如果不再盖第二次的话灯帽内热的空气冷却后压强减小,在外界大气压的作用下,下次再用时不容易拔下来
.②粗盐提纯实验中之蒸发时,要用玻璃棒不断搅拌
为防止液体受热不均匀而溅出
为防止液体受热不均匀而溅出
.(2)理解与应用
①为了验证Zn、Fe、Cu三种金属活动顺序为:Zn>Fe>Cu这一结论,下面实验设计不合理的是
D
D
.A.将Zn、Cu分别放入FeSO4溶液中
B.将相同条件下的Zn、Fe、Cu分别放入稀硫酸溶液中
C.将Fe分别放入ZnSO4、CuSO4溶液中
D.将Zn、Cu分别放入CuSO4溶液中
②甲化工厂排出的废水中含有少量氢氧化钾和硫酸钾,某实验小组对乙化工厂排出的废水测定后,决定将甲、乙两化工厂的废水按一定比例混合,所得溶液pH=7,且只含有氯化钾一种溶质溶液用作农田灌溉.乙化工厂的废水中含有的物质是(填化学式)
HCl、BaCl2
HCl、BaCl2
.分析:(1)根据第二次盖灯帽的原因和造成的后果以及蒸发溶液中玻璃棒的作用考虑本题.
(2)①利用金属活动顺序表设计实验,去验证金属的活动性强弱.氢前边的金属会与酸反应放出氢气,但氢后边的金属不会与酸反应,前边的金属会把后边的金属从其盐溶液中置换出来;
②甲化工厂的废水中含有少量氢氧化钾和硫酸钾,与乙化工厂的废水混合后,测得溶液的pH=7,且只含有氯化钾一种溶质,说明甲化工厂中的KOH转化为KCl,应和HCl反应,应和BaCl2反应生成BaSO4和KCl,则乙化工厂的废水中含有的物质是盐酸和氯化钡.
(2)①利用金属活动顺序表设计实验,去验证金属的活动性强弱.氢前边的金属会与酸反应放出氢气,但氢后边的金属不会与酸反应,前边的金属会把后边的金属从其盐溶液中置换出来;
②甲化工厂的废水中含有少量氢氧化钾和硫酸钾,与乙化工厂的废水混合后,测得溶液的pH=7,且只含有氯化钾一种溶质,说明甲化工厂中的KOH转化为KCl,应和HCl反应,应和BaCl2反应生成BaSO4和KCl,则乙化工厂的废水中含有的物质是盐酸和氯化钡.
解答:解:(1)①第一次盖灭火焰但灯帽内存有热的空气,如果不再盖第二次的话灯帽内热的空气冷却后压强减小,在外界大气压的作用下,下次再用时不容易拔下来,故答案为:第一次盖灭火焰但灯帽内存有热的空气,如果不再盖第二次的话灯帽内热的空气冷却后压强减小,在外界大气压的作用下,下次再用时不容易拔下来;
②蒸发液体过程中,为防止液体受热不均匀而溅出,所以要不断用玻璃棒搅拌,故答案为:为防止液体受热不均匀而溅出.
(2)①A、该方案中Zn能置换硫酸亚铁中的铁,说明Zn活动性比Fe强;Cu不能置换硫酸亚铁中的铁,说明Cu活动性不如比Fe强,则活动性顺序为Zn>Fe>Cu;故合理;
B、锌、铁能和稀硫酸反应,铜不能和硫酸反应,说明锌、铁的活泼性大于铜的,根据锌与硫酸反应产生的气泡快,可判断锌比铁活泼,因此三种金属的活动性顺序是Zn>Fe>Cu;故合理;
C、该方案中铁能置换硫酸铜中的铜,说明铁比铜活泼,铁不能置换硫酸锌中的锌,说明铁不如锌活泼,因此三种金属的活动性顺序是Zn>Fe>Cu;故合理;
D、该方案根据Zn能置换铜,说明Zn活动性比Cu强,但不能判断Zn与Fe、Fe与Cu的活动性强弱关系,因此不能确定Zn、Fe、Cu三种金属的活动性顺序;故不合理;故选:D;
②甲化工厂的废水中含有少量氢氧化钾和硫酸钾,与乙化工厂的废水混合后,测得溶液的pH=7,且只含有氯化钾一种溶质,说明甲化工厂中的KOH转化为KCl,应和HCl反应,应和BaCl2反应生成BaSO4和KCl,则乙化工厂的废水中含有的物质是盐酸和氯化钡,故答案为:HCl、BaCl2 .
②蒸发液体过程中,为防止液体受热不均匀而溅出,所以要不断用玻璃棒搅拌,故答案为:为防止液体受热不均匀而溅出.
(2)①A、该方案中Zn能置换硫酸亚铁中的铁,说明Zn活动性比Fe强;Cu不能置换硫酸亚铁中的铁,说明Cu活动性不如比Fe强,则活动性顺序为Zn>Fe>Cu;故合理;
B、锌、铁能和稀硫酸反应,铜不能和硫酸反应,说明锌、铁的活泼性大于铜的,根据锌与硫酸反应产生的气泡快,可判断锌比铁活泼,因此三种金属的活动性顺序是Zn>Fe>Cu;故合理;
C、该方案中铁能置换硫酸铜中的铜,说明铁比铜活泼,铁不能置换硫酸锌中的锌,说明铁不如锌活泼,因此三种金属的活动性顺序是Zn>Fe>Cu;故合理;
D、该方案根据Zn能置换铜,说明Zn活动性比Cu强,但不能判断Zn与Fe、Fe与Cu的活动性强弱关系,因此不能确定Zn、Fe、Cu三种金属的活动性顺序;故不合理;故选:D;
②甲化工厂的废水中含有少量氢氧化钾和硫酸钾,与乙化工厂的废水混合后,测得溶液的pH=7,且只含有氯化钾一种溶质,说明甲化工厂中的KOH转化为KCl,应和HCl反应,应和BaCl2反应生成BaSO4和KCl,则乙化工厂的废水中含有的物质是盐酸和氯化钡,故答案为:HCl、BaCl2 .
点评:本题考查了常见实验的注意事项、金属活动性顺序的应用和酸碱盐的性质,完成此题,可以依据已有的知识进行解答.

练习册系列答案
相关题目