题目内容
14.往盛有一定量盐酸的锥形瓶中逐滴加入氢氧化钠溶液至过量,下列图象能合理表示此过程中发生的相应变化的是( )| A. | 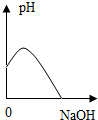 | B. |  | C. | 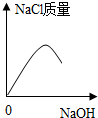 | D. | 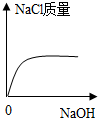 |
分析 盐酸与氢氧化钠反应生成了氯化钠和水,据此分析溶液的pH、氯化钠的变化.
解答 解:A、往盛有一定量盐酸的锥形瓶中逐滴加入氢氧化钠溶液至过量,溶液的pH会增大,不会减小,故A错误;
B、盐酸溶液的pH不一定是0.故B错误;
C、往盛有一定量盐酸的锥形瓶中逐滴加入氢氧化钠溶液至过量,生成的氯化钠的质量不会减小,故C错误;
D、往盛有一定量盐酸的锥形瓶中逐滴加入氢氧化钠溶液至过量,生成的氯化钠的质量会增多,当盐酸完全反应后,不再增多,故D正确.
故选D.
点评 本题的难度不大,了解盐酸与氢氧化钠反应时溶液的pH、氯化钠的变化是解答本题的基础.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.物质的结构决定物质的性质.下列关于物质的组成结构与性质的说法正确的是( )
| A. | 生铁和钢的性能不同,主要是由于其含碳量不同 | |
| B. | 水与过氧化氢的组成元素相同,化学性质也相同 | |
| C. | 金刚石和石墨的物理性质不同,是由于构成它们的碳原子不同 | |
| D. | 金属钠和镁的化学性质不同,主要是由于钠原子和镁原子的质子数不同 |
2.化学实验表明,向KCl溶液通电时能发生化学反应.根据质量守恒定律,一定不能得到的生成物是( )
| A. | KOH | B. | KNO3 | C. | H2 | D. | Cl2 |
9.下列推测、推断或解释、归纳正确的是( )
| A. | 食盐溶液、蔗糖溶液是$\stackrel{推断}{→}$无色的液体都是溶液 | |
| B. | 在室温下的硝酸钾饱和溶液$\stackrel{推测}{→}$此时该溶液不能再溶解其它任何物质了 | |
| C. | 氢氧化钠溶于水时温度会升高$\stackrel{归纳}{→}$ 有些物质溶解时会吸热 | |
| D. | 向两张纸片之间吹气,纸片向中间靠拢 $\stackrel{解释}{→}$ 两纸片之间空气流速增大,导致气压比纸片外侧的大气压要小 |
19.某同学从定量角度研究双氧水制取氧气的过程,对原实验进行部分改进,增加了称量操作.具体做法是:取10%的双氧水和少量的二氧化锰放入气体发生装置,并对反应前后混合物的质量进行称量,记录如下:
苦反应后,双氧水分解完全且氧气全部逸出.求:
(1)生成氧气的放质量.
(2)双氧水溶液的质量.
(3)在反应过程中,反应速率减慢(选填“加快”,“减慢”或“不变).
| 反应过程 | 反应前 | 反应后 |
| 反应前后的质量(不含容器质量)/克 | 34.3 | 32.7 |
(1)生成氧气的放质量.
(2)双氧水溶液的质量.
(3)在反应过程中,反应速率减慢(选填“加快”,“减慢”或“不变).
6. 在实验室中,小敏同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂.他们对该试剂进行定量实验分析:称取试剂19.8g放入锥形瓶中,加入30.2g的水,充分振荡,再向锥形瓶中依次滴加25g盐酸充分反应.测得部分数据与图象如下.请根据有关信息回答问题:
在实验室中,小敏同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂.他们对该试剂进行定量实验分析:称取试剂19.8g放入锥形瓶中,加入30.2g的水,充分振荡,再向锥形瓶中依次滴加25g盐酸充分反应.测得部分数据与图象如下.请根据有关信息回答问题:
(1)a的数值为125,小敏同学通过实验,得出该试剂已部分变质的结论,其依据是(通过实验数据和图象做出你的分析)滴加盐酸至100g时,开始时有二氧化碳生成,证明有碳酸钙存在,之前滴加的盐酸无现象,说明了盐酸与氢氧化钙反应,从而证明氢氧化钙存在.
(2)b的数值为2.2.
(3)计算该试剂中氢氧化钙的质量分数.(写出计算过程,结果保留一位小数)
 在实验室中,小敏同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂.他们对该试剂进行定量实验分析:称取试剂19.8g放入锥形瓶中,加入30.2g的水,充分振荡,再向锥形瓶中依次滴加25g盐酸充分反应.测得部分数据与图象如下.请根据有关信息回答问题:
在实验室中,小敏同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂.他们对该试剂进行定量实验分析:称取试剂19.8g放入锥形瓶中,加入30.2g的水,充分振荡,再向锥形瓶中依次滴加25g盐酸充分反应.测得部分数据与图象如下.请根据有关信息回答问题:| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
| 加入盐酸的质量(g) | 25 | 25 | 25 | 25 | 25 | 25 |
| 锥形瓶中物质的质量(g) | 75 | 100 | a | 150 | 172.8 | 197.8 |
(2)b的数值为2.2.
(3)计算该试剂中氢氧化钙的质量分数.(写出计算过程,结果保留一位小数)
3.下列符号中,既能表示一种元素,又能表示一个原子,还能表示一种单质的是( )
| A. | N | B. | H2 | C. | Ne | D. | O2- |