题目内容
将一定量的铁粉加入硝酸银、硝酸铜混合溶液中,完全反应后,所得滤渣加入稀盐酸无明显现象,试分析:
(1)滤渣中一定有 ;可能有 .(填金属单质化学式)
(2)滤液中一定有 ;可能有 .(填离子符号)
(1)滤渣中一定有
(2)滤液中一定有
考点:金属的化学性质,化学式的书写及意义,化学符号及其周围数字的意义
专题:金属与金属材料
分析:根据三种金属活动性强弱关系:铁>氢>铜>银,在硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,铁能与硝酸银、硝酸铜依次发生反应.由向滤渣中加入稀盐酸,无明显现象,则说明铁粉无剩余,滤渣中一定有的金属银,滤液中一定硝酸亚铁.据此分析完成填空.
解答:解:
由三种金属活动性强弱关系:铁>氢>铜>银,在硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,铁能与硝酸银、硝酸铜依次发生反应.由向滤渣中加入稀盐酸,无明显现象,则说明铁粉无剩余,滤渣中一定有金属银,滤液中一定硝酸亚铁.滤液中一定有的离子是NO3-和Fe2+;因为铁的量如果不足,则滤液中可能有Ag+、Cu2+;
故答案为:
(1)银; Cu.(2)NO3-和Fe2+; Ag+、Cu2+.
由三种金属活动性强弱关系:铁>氢>铜>银,在硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,铁能与硝酸银、硝酸铜依次发生反应.由向滤渣中加入稀盐酸,无明显现象,则说明铁粉无剩余,滤渣中一定有金属银,滤液中一定硝酸亚铁.滤液中一定有的离子是NO3-和Fe2+;因为铁的量如果不足,则滤液中可能有Ag+、Cu2+;
故答案为:
(1)银; Cu.(2)NO3-和Fe2+; Ag+、Cu2+.
点评:活动性强的金属放入活动性弱的金属的混合盐溶液中,活动性强的金属会先把活动性最弱的金属从其盐溶液中置换出来,然后再置换活动性较弱的金属.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
碳在氧气中燃烧,下列说法符合质量守恒定律的是( )
| A、2g C和9g O2生成11CO2 |
| B、3g C和8g O2生成11g CO2 |
| C、4g C和7g O2生成11gCO2 |
| D、5g C和6g O2生成11g CO2 |
下列图示中,正确的是( )
A、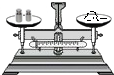 称量氯化钠 |
B、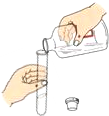 取少量液体 |
C、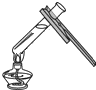 加热液体 |
D、 点燃酒精灯 |
如图是某化学反应的微观模型示意图,其中不同符号代表不同种原子.下列分析错误的是( )
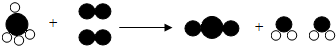

| A、该化学反应中共有两种元素 |
| B、反应的本质是原子的重新组合过程 |
| C、分子是由原子构成的 |
| D、示意图中的各物质均属于化合物 |