题目内容
海水是一种重要的自然资源(海水中含NaCl、MgCl2等物质),被誉为“国防金属”的镁主要是从海水中提取的,下面是从海水中提取金属镁的简单流程.
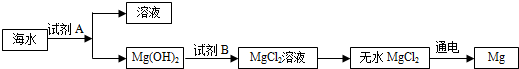
(1)从海水中获得淡水,常用的方法是 .
(2)用无水MgCl2制取Mg的化学方程式为是 .
(3)试剂A最好选用 .

(1)从海水中获得淡水,常用的方法是
(2)用无水MgCl2制取Mg的化学方程式为是
(3)试剂A最好选用
考点:对海洋资源的合理开发与利用,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的盐 化学肥料
分析:(1)海水淡化是将海水中的可溶性杂质(氯化钠、氯化镁、氯化钙等)除去的过程,可根据淡化原理进行分析解答.
(2)用无水MgCl2制取Mg,同时生成氯气,写出反应的化学方程式即可.
(3)海水中的氯化镁与碱溶液反应能生成氢氧化镁沉淀,据此进行分析解答.
(2)用无水MgCl2制取Mg,同时生成氯气,写出反应的化学方程式即可.
(3)海水中的氯化镁与碱溶液反应能生成氢氧化镁沉淀,据此进行分析解答.
解答:解:(1)海水淡化是将海水中的可溶性杂质(氯化钠、氯化镁、氯化钙等)除去的过程,从海水中获得淡水,常用的方法是蒸馏.
(2)用无水MgCl2制取Mg,同时生成氯气,反应的化学方程式为:MgCl2
Mg+Cl2↑.
(3)熟石灰(氢氧化钙的俗称)显碱性,能和氯化镁反应生成氢氧化镁沉淀,且氢氧化钙的价格比较便宜,故试剂A最好选用熟石灰.
故答案为:(1)蒸馏;(2)MgCl2
Mg+Cl2↑;(3)熟石灰.
(2)用无水MgCl2制取Mg,同时生成氯气,反应的化学方程式为:MgCl2
| ||
(3)熟石灰(氢氧化钙的俗称)显碱性,能和氯化镁反应生成氢氧化镁沉淀,且氢氧化钙的价格比较便宜,故试剂A最好选用熟石灰.
故答案为:(1)蒸馏;(2)MgCl2
| ||
点评:本题难度不大,掌握海水淡化的原理、盐的化学性质、化学方程式的书写方法是正确解答本题的关键.

练习册系列答案
相关题目
“垃圾是放错了地方的资源”,应分类回收利用.生活中废弃的塑料袋、废纸、旧橡胶制品等属于( )
| A、无机物 | B、有机物 |
| C、盐类 | D、糖类 |
关于化学反应A+B=C+D,下列说法中正确的是( )
| A、若生成物C和D分别是盐和水,则反应物一定是酸和碱 |
| B、若C是单质、D为化合物,则A和B中一定有一种是单质,一种是化合物 |
| C、若B是酸,则C和D一定有一种是化合物 |
| D、若A、B各取10g混合,使其充分反应,则C、D质量的总和一定等于20g |
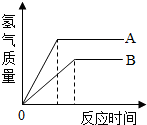 等质量的A、B两种金属,分别与相同质量分数的足量稀盐酸反应(已知A、B在生成物中均为+2价),生成氢气的质量与反应时间的关系如图所示,下列叙述正确的是( )
等质量的A、B两种金属,分别与相同质量分数的足量稀盐酸反应(已知A、B在生成物中均为+2价),生成氢气的质量与反应时间的关系如图所示,下列叙述正确的是( )| A、产生氢气的速率是 B>A |
| B、相对原子质量是 B>A |
| C、生成氢气的质量是 B>A |
| D、金属活动性顺序是 B>A |
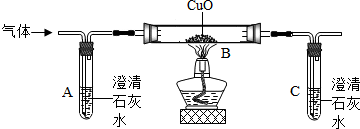 不少同学都被蚊虫叮咬过,感觉又痛又痒.同学们从化学课上知道:蚊虫叮咬时能在人的皮肤内分泌出蚁酸刺激皮肤.课外兴趣小组同学决定对蚁酸进行探究.
不少同学都被蚊虫叮咬过,感觉又痛又痒.同学们从化学课上知道:蚊虫叮咬时能在人的皮肤内分泌出蚁酸刺激皮肤.课外兴趣小组同学决定对蚁酸进行探究.