题目内容
10. 梧州市某中学化学兴趣小组的同学到超市购买锡纸用于烧烤,同学们看见商品标签上表明锡纸的材质为“铝箔”.
梧州市某中学化学兴趣小组的同学到超市购买锡纸用于烧烤,同学们看见商品标签上表明锡纸的材质为“铝箔”.【提出问题】锡纸的材质到底是锡还是铝呢?小吴认为可以把锡纸放入盐酸中观察是否有气体放出来区别是锡还是铝,小周同学认为这样不能区别,理由是锡和铝都能与盐酸反应生成氢气.小施查阅资料发现锡的熔点为232℃,而铝的熔点为660℃,他用加热的方法区别出锡纸的材质是铝不是锡,接着同学们对铝这种金属进行探究.
【探究活动一】铝的含量分析
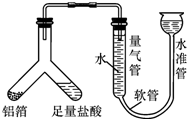
(1)小施用如图装置测定铝箔中金属铝的含量,检查该装置气密性的操作是从水准管一端注入水,待水准管和量气管出现较大高度差为止,静止几分钟,两侧高度差不缩小,证明装置气密性好.
(2)若测定进入量气管的气体体积为100mL(氢气的密度为0.09g/L),铝箔中金属铝的质量为0.081g(铝箔中只有铝能与盐酸反应生成气体).
【探究活动二】铝箔燃烧
同学们做铝箔燃烧的实验.小吴用坩埚钳夹持一小块铝箔放在酒精灯火焰上,轻轻晃动,观察到铝箔熔化,失去了光泽,但铝箔并不燃烧;小周另取一块铝箔,用砂纸仔细打磨,再用坩埚钳夹持放在酒精灯的火焰上,观察到铝箔仍不能燃烧.
(1)小施同学认为铝箔不能在空气中燃烧是因为铝与氧气反应生成一层致密的氧化铝薄膜附在铝的表面,阻止反应的进行,这也是铝箔抗腐蚀性强的原因.
(2)小施同学改进了实验,让铝箔燃烧并发出耀眼的白光,小施同学的实验方案是将铝箔卷曲,尖端夹一根火柴,将火柴引燃后,把火柴和铝箔一起伸入到盛有氧气的集气瓶中即可观察到铝箔燃烧并发出耀眼的白光.
【探究活动三】小吴将打磨后的铝片与铜盐溶液反应,现象如下:
| 实验一:4mL8%CuSO4溶液 | 实验二:4mL8%CuCl2溶液 | |
| 实验 现象 | 短时间内无变化,一段时间后铝片上才出现少量红色的铜 | 铝片上迅速有红色的铜出现 |
(2)对比两个实验,小周推测对铝与铜盐溶液的反应可能有促进作用的离子是Cl-(填离子符号),为了验证此推测,小施向实验一的CuSO4溶液中加入1gNaCl(填化学式)固体,立即观察到铝片上出现大量红色的铜.
分析 根据金属的性质、检查装置气密性的方法、铝易被氧气氧化、金属与盐溶液反应的特点以及化学方程式的书写进行分析解答即可.
解答 解:【提出问题】由于锡和铝都能与盐酸反应生成氢气,故不能用加盐酸的方法鉴别锡和铝;利用熔点的不同可以采用加热的方法鉴别,故填:锡和铝都能与盐酸反应生成氢气;加热;
【探究活动一】(1)要检查该装置的气密性,可以从水准管一端注入水,待水准管和量气管出现较大高度差为止,静止几分钟,两侧高度差不缩小,证明装置气密性好,故填:从水准管一端注入水,待水准管和量气管出现较大高度差为止,静止几分钟,两侧高度差不缩小,证明装置气密性好;
(2)产生的氢气体积为100mL,即0.1L,氢气的密度为0.09g/L,故氢气的质量为:0.1L×0.09g/L=0.009g,设铝的质量为x,则有:
2Al+6HCl═2AlCl3+3H2↑
54 6
x 0.009g
$\frac{54}{6}=\frac{x}{0.009g}$
x=0.081g
故填:0.081;
【探究活动二】(1)铝的化学性质很活泼,易被氧气氧化生成致密的氧化铝保护膜,阻止反应的进行,故填:铝与氧气反应生成一层致密的氧化铝薄膜附在铝的表面,阻止反应的进行;
(2)要使铝箔燃烧,可以用火柴引燃,然后伸进盛有氧气的集气瓶中,故填:将铝箔卷曲,尖端夹一根火柴,将火柴引燃后,把火柴和铝箔一起伸入到盛有氧气的集气瓶中即可观察到铝箔燃烧并发出耀眼的白光;
【探究活动三】(1)铝与氯化铜反应生成氯化铝和铜,故填:2Al+3CuCl2═2AlCl3+3Cu;
(2)对比两个实验,氯化铜溶液中能快速出现红色的物质,说明对铝与铜盐溶液的反应可能有促进作用的离子是氯离子;可以才硫酸铜溶液中加入含有氯离子的氯化钠来进行实验,故填:Cl-;NaCl.
点评 本题考查的是金属化学性质的实验探究,完成此题,可以依据已有的金属的性质结合物质间反应的实验现象进行.

 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案 名题金卷系列答案
名题金卷系列答案| A. | 发现燃气泄漏,点火检查出泄漏处 | |
| B. | 用食醋除去热水瓶中的水垢 | |
| C. | 熟石灰用于改良酸性土壤 | |
| D. | 炒菜时油锅着火,可用锅盖盖灭火焰 |
【提出猜想】A.只有CO2 B.只有CO C.既有CO2,也有CO
【查阅资料】微量CO遇到浸有磷钼酸溶液的氯化钯黄色试纸,试纸立即变蓝;而CO2遇该试纸不变色
【设计方案】化学兴趣小组在老师的指导下,设计如图所示实验,通过观察装置B、装置C的实验现象,验证猜想.

【实验探究】请你帮助他们写成实验报告.
| 实验步骤 | 实验现象 | 实验结论及化学方程式 |
| 点燃酒精灯加热,随即打开弹簧夹,通入干燥的空气. 观察装置B、装置C中的现象 | 装置B中的现象是: 黄色试纸变蓝 装置C中的现象是: 澄清石灰水变浑浊 | 聚乙烯塑料在空气中燃烧,生成碳的氧化物中,既有CO2,也有CO. 装置C中反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O |
| A. | 工业上要用大量的水来洗涤、溶解、加热和冷却 | |
| B. | 水可以用来发电,作为原料来制造化肥等产品 | |
| C. | 工农业生产用被污染的水并不会降低产品的质量 | |
| D. | 交通运输离不开水,故称长江是水上运输的“黄金渠道” |