题目内容
25℃时,向20.0mL质量分数为30%的盐酸中滴加氢氧化钠溶液,溶液的pH与所加氢氧化钠溶液的体积如图所示,下列有关叙述正确的是
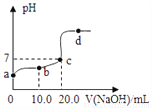
A. d点对应的溶液中溶质是NaCl和NaOH
B. 所用氢氧化钠溶液的质量分数一定为30%
C. 向b点对应的溶液中滴加石蕊溶液,溶液呈无色
D. b、d点对应溶液的pH:b>d
A 【解析】A. d点表示氢氧化钠过量,对应的溶液中溶质NaCl和NaOH,正确;B. 向20.0mL质量分数为30%的盐酸中滴加氢氧化钠溶液,由图可知刚好完全反应时,需要氢氧化钠溶液20.0mL,NaOH +HCl == NaCl + H2O,由方程式可知氢氧化钠和氯化氢的质量比为40:36.5,故所用氢氧化钠溶液的质量分数一定大于30%,错误;C. b点氢氧化钠不足,盐酸有剩余,对应的溶... 轻松课堂单元期中期末专题冲刺100分系列答案
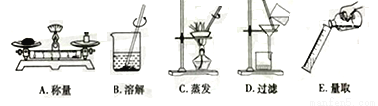
轻松课堂单元期中期末专题冲刺100分系列答案化学实验和科学探究都离不开实验装置。根据下列装置回答问题:

(1)以上A和B装置都可以用于制取氧气,写出用B装置制取氧气的化学方程式_______;
(2)可用于收集氢气的装置是______(填写序号字母)。
(3)科学探究
(查阅资料)小玲同学查阅资料发现:过氧化钙(CaO2)能分别与水、二氧化碳反应。
(猜想)①过氧化钙与水反应生成氢氧化钙和氧气。
②过氧化钙在空气中久置生成的物质可能是碳酸钙或氢氧化钙或二者的混合物。
(实验探究)
实验一:选用上述实验装置B进行过氧化钙与水反应的实验,收集一试管气体,将带火星的木条伸入试管中,木条复燃;取反应后的溶液置于试管中,充分振荡后再滴入_______(填写一种指试剂的名称)试液,发现溶液变成红色,说明猜想①正确,反应的化学方程式是______。
实验二:为探究猜想②是否正确,小玲设计了如下实验,请你帮助她完成表格中的空白内容:
实验步骤 | 实现现象 | 结论 |
a.取在空气中久置的少量固体于试管中,加足量水 | 未见固体明显溶解 | |
b.向试管中滴加几滴紫色石蕊试液 | 未见明显颜色变化 | 不存在氢氧化钙 |
C. ______ | ______ | 固体成分是碳酸钙 |
实验步骤C中发生反应的化学方程式是______。
D和E 酚酞 另取少量固体于试管中滴加稀盐酸 产生气泡,固体逐渐溶解 【解析】(1)A装置适用于固体和固体加热条件下制取气体,B装置适用于固体和液体常温下制取气体,过氧化氢法制氧气用B装置,反应的化学方程式2H2O22H2O+O2↑;(2)氢气难溶于水,可用排水法收集,使用装置E;氢气的密度比空气的小,可以用向下排空气法收集,可用装置D;【实验探究】实验一:选用过氧化钙与水反应,收集一试管气...实验室中有一包白色粉末,可能是碳酸钠,也可能是氧化钙或氢氧化钙。为确定其组成,某同学设计了以下实验方案进行探究,请你按要求帮助完成探究活动。
(1)提出假设:
假设① 白色粉末是碳酸钠
假设② 白色粉末是氧化钙
假设③ 白色粉末是氢氧化钙
(2)设计实验,通过实验分析进行判断并填空:
假设 | 设计的相关实验操作 | 实验中观察到的现象 | 假设是否成立 |
① | 取一定量粉末加入稀盐酸 | ____________ | 假设①不成立 |
② | 取一定量粉末溶于水 | 溶液浑浊且温度升高 | 假设②成立 |
③ | 取一定量粉末溶于水,静置后取上层清液再通入二氧化碳 | 没有沉淀产生 | 假设③______ |
(3)实验后思考:假定这包白色粉末是混有少量氧化钙的碳酸钠粉末,将混合物溶于水可观察到的现象是____________;若恰好完全反应,将反应后的混合物进行分离,分离的方法是________;再将分离后的溶液蒸干,得到的固体物质是______(填化学式)。
无气泡产生 , 不成立 , 产生白色沉淀 , 过滤 , NaOH (填化学式) 【解析】(2)①取一定量的粉末加盐酸无气泡产生,说明粉末中没有碳酸钠,故假设①不成立;②取一定量粉末溶于水,溶液浑浊且温度升高,说明粉末中含氧化钙,故假设②成立, ③取一定量粉末溶于水,静置后取上层清液再通入二氧化碳,没有沉淀产生,说明粉末中不含氢氧化钙,故假设③不成立;(3)氧化钙可与水反应生成氢氧化钙,生成...

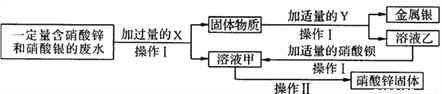


 Si +2CO↑,该反应属于
Si +2CO↑,该反应属于
