题目内容
5.氯气(Cl2)是一种重要的化工原料.在实验室,利用高锰酸钾固体与X的溶液反应可制得氯气,反应的化学方程式为:2KMnO4+□X═2KCl+2MnCl2+5C12↑+8H2O,关于该实验,下列有关说法正确的是( )| A. | 该反应的化学方程式中,X的化学计量数是12 | |
| B. | X由三种元素组成,其中一定含有氯元素 | |
| C. | X中所含元素的质量比为l:35.5 | |
| D. | 该实验发生装置与实验室用高锰酸钾制氧气的发生装置相同 |
分析 根据质量守恒定律分析解答.
解答 解:根据质量守恒定律,反应前后原子的种类和个数不变,
反应前:2K,2Mn,8O
反应后:2K,16Cl,2Mn,16H,8O
故X的化学式为:HCl,计量数为16;氢元素与氯元素的质量比为:1:35.5,故AB错误,C正确;
该反应为固液常温型,实验室用高锰酸钾制氧气的发生装置为固体加热型,装置不同,故D错误;
故选C.
点评 熟练掌握质量守恒定律的意义是正确解答本题的关键.

练习册系列答案
 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
13.推理是一种重要的化学思维方法,以下推理合理的是( )
| A. | 酸碱发生中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 | |
| B. | 酸溶液中都含有氢离子,所以含有氢元素的物质一定是酸 | |
| C. | 有机物都含有碳元素,所以含有碳元素的化合物一定是有机物 | |
| D. | 化合物是由不同元素组成的纯净物,所以只含一种元素的物质一定不是化合物 |
17.除去下列物质中的少量杂质,所选试剂及操作方法都正确的是( )
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | Cu(CuO) | 足量稀硫酸 | 过滤、洗涤、干燥 |
| B | NaCl(KNO3) | 水 | 溶解、降温结晶、过滤 |
| C | NaCl(MgCl2) | 过量NaOH溶液 | 过滤、蒸发结晶 |
| D | CO2(CO) | 足量O2 | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
14.某同学想探究贝壳中碳酸钙的质量分数,取贝壳25g高温加热,完全反应后称量固体剩余物质质量为16.2g,则贝壳中碳酸钙的质量分数为( )
| A. | 90% | B. | 95% | C. | 80% | D. | 70% |
15.灼烧时,火焰呈黄色的是( )
| A. | KCl | B. | NH4NO3 | C. | CuCl2 | D. | NaNO3 |

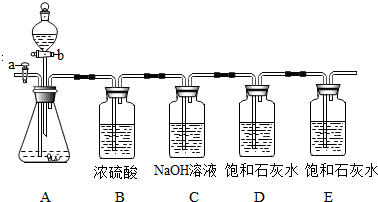
 某教师设计的创新实验装置图如图,请完成下列探究:
某教师设计的创新实验装置图如图,请完成下列探究: