题目内容
20.按如表提供的信息,完成下列填空: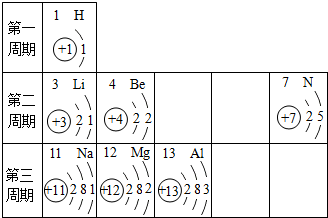
(1)H+核外电子数为0;
(2)写出一条第三周期元素原子的核外电子排布规律同一周期的元素的原子,核外电子层数相同;同一周期元素的原子,从左至右最外层电子数依次增大等;
(3)第7号元素与第12号元素的原子形成化合物的化学式为Mg3N2;
(4)X、Y、Z、W元素表示4种物质,它们的微观示意图如图:
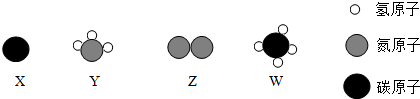
物质X和Y在高温和催化剂条件下反应生成Z和W两种物质,反应的化学方程式为3C+4NH3$\frac{\underline{\;催化剂\;}}{高温}$2N2+3CH4.
分析 (1)根据氢离子的形成来分析;
(2)根据同一周期元素原子核外电子排布的规律可从周期数与电子层数的关系、最外层电子数的变化进行分析解答.
(3)确定元素种类,然后根据化学式的写法来分析;
(4)根据微观反应示意图的意义来分析.
解答 解:(1)氢原子的核外只有一个电子,失去后形成氢离子;故填:0;
(2)在元素周期表中,处于同一周期的元素的原子,核外电子层数相同;同一周期元素的原子,从左至右最外层电子数依次增大(合理即可).
故答案为:同一周期的元素的原子,核外电子层数相同;同一周期元素的原子,从左至右最外层电子数依次增大等.
(3)7号是氮元素,常显-3价,12号是镁元素,常显+2价,二者组成的化合物是氮化镁,其化学式为Mg3N2;故答案为:Mg3N2;
(4)由微观反应示意图可知,该反应是碳和氨气在高温和催化剂条件下反应生成氮气和甲烷;故答案为:3C+4NH3$\frac{\underline{\;催化剂\;}}{高温}$2N2+3CH4.
点评 本题难度不大,考查学生灵活运用元素周期表的信息、变化规律等进行分析、解题的能力.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目
10.地壳中含量最多的元素是( )
| A. | Al | B. | Fe | C. | O | D. | Si |
11.对以下四种粒子的结构示意图,分析错误的是( )


| A. | ①②属于同一种元素 | B. | ①④的化学性质相似 | ||
| C. | ①得到电子可形成③ | D. | ②③表示不同种离子 |
15.对宏观事实的微观解释错误的是( )
| A. | 温度升高,水银柱上升,是因为汞原子变大了 | |
| B. | 缉毒犬能发现毒贩,是因为分子是不断运动的 | |
| C. | 稀有气体能做保护气,是因为构成稀有气体的原子最外层达到稳定结构 | |
| D. | 稀盐酸和稀硫酸具有相似的化学性质是因为他们解离出的阳离子都是H+ |
5.下列有关水的叙述正确的是( )
| A. | 煮沸可以使硬水软化 | B. | 地球表面淡水资源非常丰富 | ||
| C. | 水可以溶解任何物质 | D. | 明矾净水的作用是杀菌消毒 |
9.下列有关“一定”的叙述正确的是( )
| A. | 构成物质的分子、原子等粒子一定在不停地运动 | |
| B. | 灭火一定要同时破坏燃烧的三个条件 | |
| C. | 硬水经过滤后一定会变成软水 | |
| D. | 铁制品与氧气或水接触一定会锈蚀 |
 .
.