题目内容
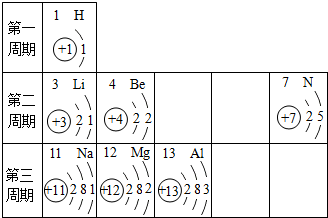
8.学习化学使我们从五彩缤纷的宏观世界步入了充满神奇色彩的微观世界.(1)我们身边有各种各样的物质,例如铜、氧气、熟石灰、金刚石、乙醇等,它们都是由不同微粒构成的.请选择上述物质填空(每空只填一种物质):
分子构成的物质氧气;原子构成的物质铜.
(2)学习完“原子的构成”之后,小英幻想自己变成一个进入原子内部的微粒,写了如下短文.
我想象中的原子结构
进入镁原子,我发现①原子是由原子核与核外电子构成的,②原子核相比较原子的体积竟然那么小.③核外的12个电子按固定轨道围绕原子核作高速运动,④我试着去搬动它们,发现电子的质量与原子核的质量差不多…
我走出幻境,画出了镁原子结构示意图
 .
.小英对原子结构的认识有些是错误的,指出文中有错误的一句话④(填句子前的序号).文中提到的原子在化学变化中易失去电子(填“得到”或“失去”).
(3)同学们已经学会从微观角度认识物质的变化,下列变化中微粒种类发生了改变的是ad(填字母,符合题意的选项都选).
a.食物腐烂 b.冰雪融化 c.酒精挥发 d.红磷燃烧
(4)我们接触过很多化学变化,如“氢气燃烧”、“铁和硝酸银溶液反应”、“稀盐酸与澄清石灰水反应”等,这些变化的微观本质各不相同.
①写出上述三个反应中任意两个反应的化学方程式:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;Fe+2AgNO3═Fe(NO3)2+2Ag.
②从上述三个反应中任取一个写出其微观本质:氢分子分解成氢原子,氧分子分解成氧原子,每2个氢原子和1个氧原子结合成1个水分子,大量的水分子聚集成水.
分析 (1)根据金属和大多数固态非金属单质等由原子构成,有些物质是由分子构成的,如水、气态非金属单质等,有些物质是由离子构成的,如氯化钠;
(2)根据电子的质量很小,可以忽略不计,根据原子结构示意图中,最外层电子数小于4个,易失去电子解答;
(3)化学变化是产生新物质的变化,物理变化是不产生新物质的变化.二者的本质区别是有无新物质产生.用分子观点解释化学变化产生了新分子,物理变化没有产生新分子;
(4)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.在化学变化中分子可分,原子不可分.变化的实质是分子分解成原子,原子再结合成新分子.
解答 解:(1)分子构成的物质有氧气、乙醇;原子构成的物质有铜、金刚石;
(2)电子的质量很小,可以忽略不计,文中有错误的一句话④;原子结构示意图中,最外层电子数小于4个,在化学变化中易失去电子;
(3)用分子观点解释化学变化产生了新分子,物理变化没有产生新分子.分子种类发生改变的一定是化学变化.
a、食物腐烂生成新物质,是化学变化.
b、冰雪融化没有产生新物质,是物理变化.
c、酒精挥发没有产生新物质,是物理变化.
d、红磷燃烧成新物质五氧化二磷,是化学变化.
(4)
①氢气燃烧生成水,反应的化学方程式为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
铁和硝酸银溶液反应生成硝酸亚铁和银,反应的化学方程式为:Fe+2AgNO3═Fe(NO3)2+2Ag.
②氢分子分解成氢原子,氧分子分解成氧原子,每2个氢原子和1个氧原子结合成1个水分子,大量的水分子聚集成水.
答案:
(1)氧气;铜;
(2)④;失去;
(3)ad;
(4)①2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.Fe+2AgNO3═Fe(NO3)2+2Ag.
②氢分子分解成氢原子,氧分子分解成氧原子,每2个氢原子和1个氧原子结合成1个水分子,大量的水分子聚集成水
点评 掌握分子的基本性质(可以简记为:“两小运间,同同不不”)及利用分子的基本性质分析和解决问题的方法是解答此类题的关键.考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

| A. | 用甲醛溶液浸泡海产品,以延长保质期 | |
| B. | 为预防缺碘性疾病,可食用适量海带 | |
| C. | 食用“加铁酱油”,可补充铁元素,预防缺铁性贫血 | |
| D. | 为使发面食品松软可口,制作时可添加适量碳酸氢钠 |
| 实验步骤 | 实验操作 | 实验现象 |
| 步骤1 | 取样品加入足量水,充分振荡,静置 | 有白色沉淀产生 |
| 步骤2 | 过滤后,往滤渣中加入过量的稀盐酸 | 沉淀全部溶解,并有气体产生 |
(2)通过探究,得出的结论是样品中一定有Ba(NO3)2、Na2CO3,一定没有Na2SO4,可能有NaNO3.
| A. | 葡萄糖 | B. | 液氨 | C. | 氯酸钾 | D. | 一氧化碳 |
| A. | 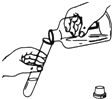 倾倒液体 | B. | 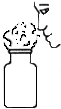 闻气体气味 | C. |  读液体体积 | D. |  稀释浓硫酸 |
| A. | 角鲨烯是由碳、氢两种元素组成的 | |
| B. | 角鲨烯是由角鲨烯分子构成的 | |
| C. | 角鲨烯分子中碳原子和氢原子的原子个数比为3:5 | |
| D. | 角鲨烯中氢元素的质量分数为62.5% |
【提出问题】硫酸铜溶液是不是此反应的催化剂?硫酸铜溶液的体积对此实验有影响吗?
【设计并实验】室温下,小明将过量、表面积相同已打磨的铝片分别加入到6份30mL10%稀盐酸中,并在每份中加入不同体积的硫酸铜饱和溶液,记录获得相同体积氢气的时间,从而确定产生氢气的速率.
| 实验混合溶液 | 1 | 2 | 3 | 4 | 5 | 6 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | 10 | 20 |
| 水/mL | 20 | 19.5 | 17.5 | V | 10 | 0 |
(2)写出铝和稀盐酸反应的化学方程式:2Al+6HCl═2AlCl3+3H2↑.
(3)定量收集氢气体积可用如图c(填写字母序号)装置.
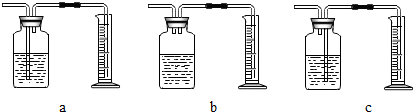
【实验现象】随着硫酸铜溶液体积的增加,产生氢气的速率先加快后明显减慢,且铝片表面附着的红色物质逐渐增加.
【结论与解释】
(4)随着硫酸铜溶液体积的增加,反应速率明显变慢可能的原因是部分铝和硫酸铜溶液发生了置换反应.
(5)根据实验现象小明认为硫酸铜溶液不是此反应的催化剂,其原因是硫酸铜质量发生了改变且和铝发生了反应.
【实验反思】加速铝和稀盐酸反应速率还可以采取的措施是提高温度,增大盐酸浓度等(写出一点).
【实验拓展】根据上述实验,小明认为是盐中的金属离子影响了铝和稀盐酸的反应速率;为了研究不同金属离子对反应的影响,小明同学继续实验,取过量表面积相同的铝片和30mL10%稀盐酸混合后加入不同的盐溶液,实验现象如表(加号越多,代表反应速率越快):
| 实验1 | 实验2 | 实验3 | 实验4 | 实验5 | |
| 加入试剂0.5mL | 水 | 5%NaCl溶液 | 5%Mg2(NO)3溶液 | 5%FeSO4溶液 | 5%CuSO4溶液 |
| 产生气泡速率 | + | + | + | ++ | +++ |
(7)上述实验设计存有缺陷,该缺陷是;改进实验后,仍符合上表中的实验现象,可得到的结论是:
①Na+、Mg2+对实验效果没有明显效果;
②Fe2+、Cu2+能加快铝和稀盐酸反应的速率,且Cu2+效果最好.
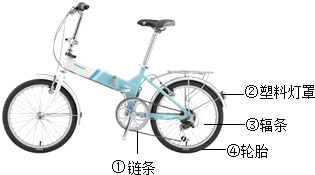 生活中处处有化学,请用所学知识回答下列问题:
生活中处处有化学,请用所学知识回答下列问题: