题目内容
7.我国著名化学家侯德榜发明的“侯氏制碱法”.是向饱和食盐水中通入过量氨气,再通入过量二氧化碳,即可析出NaHCO3固体,将其加热得到纯碱.反应的化学方程式为:NaCl+NH3+CO2+H2O═NaHCO3+NH4Cl、2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑由上述信息可知:NaHCO3常温下溶解度较小;若Na2CO3中混有NaHCO3杂质,可用加热方法将杂质除去.
分析 向饱和食盐水中通入过量氨气,再通入过量的二氧化碳,即可析出NaHCO3固体,说明NaHCO3常温下的溶解度减小;
碳酸氢钠受热分解生成碳酸钠、水和二氧化碳;
碳酸钠的热稳定性强,受热不容易分解.
解答 解:因为向饱和食盐水中通入过量氨气,再通入过量的二氧化碳,即可析出NaHCO3固体,说明NaHCO3常温下的溶解度减小;
碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,说明碳酸氢钠受热易分解;
若Na2CO3中混有NaHCO3杂质,可用加热方法将杂质除去.
故填:小;加热.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
18.通过下列实验和现象不能得出相应结论的是( )
| 选项 | A | B | C | D |
| 实 验 |  |  |  |  |
| 实验 现象 | 热水中未燃烧的白磷,在通入氧气后燃烧 | 高锰酸钾溶于水,几乎不溶于汽油 | 乙中试管内的液面高于甲中试管内的液面 | 铜片上留下划痕 |
| 实验 结论 | 燃烧需要氧气 | 物质的溶解性 只与溶剂的种 类有关 | NaOH与CO2发生了反应 | 黄铜的硬度 比铜大 |
| A. | A | B. | B | C. | C | D. | D |
18.下列说法不正确的是( )
| A. | 稀溶液也可能是饱和溶液 | |
| B. | 用汽油乳化除去试管内壁的油脂 | |
| C. | 同一种物质在不同溶剂中的溶解性不同 | |
| D. | 冬天,在汽车水箱里加入少量乙二醇可以降低水的凝固点 |
2.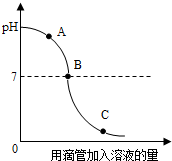 实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示曲线.下列有关该实验事实的说法正确的是( )
实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示曲线.下列有关该实验事实的说法正确的是( )
 实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示曲线.下列有关该实验事实的说法正确的是( )
实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示曲线.下列有关该实验事实的说法正确的是( )| A. | A点时溶液呈酸性 | |
| B. | B点表示盐酸和氢氧化钠恰好完全反应 | |
| C. | C点时,溶液中的溶质只有氯化钠 | |
| D. | 该实验是将氢氧化钠溶液滴入盐酸中 |
12.正确的实验操作是科学探究成功的基础,下列实验操作正确的是( )
| A. |  装入块状固体 | B. |  滴加液体药品 | C. |  倾倒液体药品 倾倒液体药品 | D. |  测定溶液的pH |
16.下列关于水的说法错误的是( )
| A. | 无色透明的水均可直接饮用 | B. | 用肥皂水可检验硬水和软水 | ||
| C. | 用活性炭可除去水中的异味 | D. | 通过蒸馏得到的水是蒸馏水 |
 如图是A、B、C三种物质的溶解度曲线,据图回答:
如图是A、B、C三种物质的溶解度曲线,据图回答: 通过分析实验结果推断物质的组成,是研究物质的一种方法.探究水的组成就是利用了这种方法.电解水实验如图所示.
通过分析实验结果推断物质的组成,是研究物质的一种方法.探究水的组成就是利用了这种方法.电解水实验如图所示. 如图是测定空气中氧气含量的实验装置图.实验测得硬质玻璃管的容积为25mL,反应前后注射器中空气体积分别为15mL和9mL.
如图是测定空气中氧气含量的实验装置图.实验测得硬质玻璃管的容积为25mL,反应前后注射器中空气体积分别为15mL和9mL.