题目内容
20.将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸质量增加而发生变化,如图所示.有关叙述中错误的是( )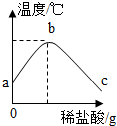
| A. | 从a到b过程中,烧杯中溶液的pH逐渐减小 | |
| B. | b点表示氢氧化钠和盐酸恰好完全反应 | |
| C. | c点表示所得溶液中溶质只有NaCl | |
| D. | 稀盐酸与氢氧化钠溶液发生的反应是放热反应 |
分析 根据图象可以看出:随着盐酸的加入温度在逐渐上升,说明稀盐酸与氢氧化钠溶液发生的反应是放热反应;A到B的过程中温度逐渐升高,B点对于温度是个转折点,对于反应进程也是个转折点;B到C的过程的反应实质,加入的稀盐酸逐渐增多,稀盐酸过量,可以据此进行分析判断.
解答 解:A、由图示可知,a到b过程中,氢氧化钠逐渐减少,碱性减弱,故pH值逐渐减小,故选项说法正确.
B、根据图象可以看出,随着稀盐酸的加入,温度逐渐升高,在b点前后温度是两种情况,b点温度最高,b点表示酸碱恰好完全反应,故选项说法正确.
C、b到c的过程中,是盐酸完全中和完氢氧化钠后继续加入稀盐酸,稀盐酸过量,故c点溶液中的溶质含有NaCl和HCl,故选项说法错误.
D、图象可以看出:随着盐酸的加入温度在逐渐上升,说明稀盐酸与氢氧化钠溶液发生的反应是放热反应,故选项说法正确.
故选:C.
点评 本题难度不是很大,本题主要考查了结合图象考查了中和反应的应用,理解图象的含义、掌握中和反应的实质是正确解答本题的关键.

练习册系列答案
相关题目
1.类推和推理是重要的学习方法.下列推理中正确的是( )
| A. | 明矾和二氧化氯均可用作净水剂,所以净水原理相同 | |
| B. | 组成CO和CO2的元素相同,但它们的分子构成不同,所以它们的化学性质不同 | |
| C. | NaOH和CaO溶于水时均能放出热量,是因为它们都能和水发生反应 | |
| D. | 浓盐酸、浓硫酸敞口放置后质量分数都会变小,是因为它们都有挥发性 |
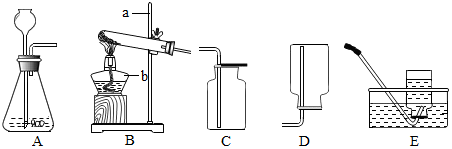
8.实验室常用的制取气体的发生装置如下:
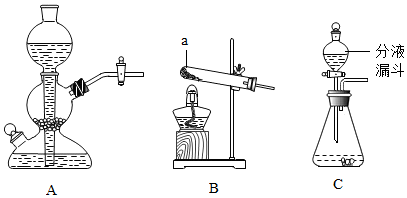
①仪器a的名称是试管;搭建B装置时,酒精灯应在固定仪器a之前(选填“前”或“后”)放置.
②实验室用过氧化氢溶液和二氧化锰混合制取氧气,反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
③在实验室制取二氧化碳的研究中,进行了如下实验:
Ⅰ.上述实验中反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑.
Ⅱ.若要研究盐酸浓度大小对反应的影响,可选择实验甲与乙对照(选填实验编号)
Ⅲ.除盐酸的浓度外,上述实验研究的另一个影响反应的因素是大理石的状态.
Ⅳ.研究发现酸的浓度越大,产生气体的速度越快,与甲比较,对丁分析正确的是ad(选填编号)
a.反应更为剧烈
b.最终剩余溶液的质量更小
c.产生二氧化碳的质量更大
d.粉末状大理石利用率更高
④表中的两个实验,尽管在原料状态、发生装置等方面存在差异,却都能控制气体较平稳的产生.请从实验目的、原理、原料、装置、操作等方面思考后,具体阐述每个实验中气体较平稳产生的最主要的一个原因.

①仪器a的名称是试管;搭建B装置时,酒精灯应在固定仪器a之前(选填“前”或“后”)放置.
②实验室用过氧化氢溶液和二氧化锰混合制取氧气,反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
③在实验室制取二氧化碳的研究中,进行了如下实验:
| 甲 | 乙 | 丙 | 丁 | |
| 大理石 | mg,块状 | mg,块状 | mg,粉末状 | mg,粉末状 |
| 盐酸(过量) | wg,稀盐酸 | wg,浓盐酸 | wg,稀盐酸 | wg,浓盐酸 |
Ⅱ.若要研究盐酸浓度大小对反应的影响,可选择实验甲与乙对照(选填实验编号)
Ⅲ.除盐酸的浓度外,上述实验研究的另一个影响反应的因素是大理石的状态.
Ⅳ.研究发现酸的浓度越大,产生气体的速度越快,与甲比较,对丁分析正确的是ad(选填编号)
a.反应更为剧烈
b.最终剩余溶液的质量更小
c.产生二氧化碳的质量更大
d.粉末状大理石利用率更高
④表中的两个实验,尽管在原料状态、发生装置等方面存在差异,却都能控制气体较平稳的产生.请从实验目的、原理、原料、装置、操作等方面思考后,具体阐述每个实验中气体较平稳产生的最主要的一个原因.
| 目的 | 原料 | 发生装置 | 气体较平稳产生的最主要的一个原因 |
| 制取二氧化碳 | 块状大理石稀盐酸 | A | 固体药品的状态和溶液的浓度有关 |
| 制取氧气 | 粉末状二氧化锰3%的过氧化氢溶液 | C | 二氧化锰起催化作用 |
12.一定条件下,一氧化碳和木炭都能与氧化铜反应,下列叙述不正确的是( )
| A. | 反应都有CO2气体生成 | B. | 反应都有红色固体生成 | ||
| C. | 反应类型都是置换反应 | D. | 一氧化碳和木炭都具有还原性 |
10.2016年诺贝尔化学奖授予在“分子机器的设计与合成”领域作出贡献的三位科学家.“分子机器”是指在分子层面上设计开发出来的“最小机器”,向其提供能量可移动并执行特定任务.下列说法正确的是( )
| A. | 分子机器是由原子构成的 | |
| B. | 分子机器的定向运动属于化学变化 | |
| C. | 分子机器的运动无需消耗能量 | |
| D. | 在普通光学显微镜下能看到分子机器 |