题目内容
1.类推和推理是重要的学习方法.下列推理中正确的是( )| A. | 明矾和二氧化氯均可用作净水剂,所以净水原理相同 | |
| B. | 组成CO和CO2的元素相同,但它们的分子构成不同,所以它们的化学性质不同 | |
| C. | NaOH和CaO溶于水时均能放出热量,是因为它们都能和水发生反应 | |
| D. | 浓盐酸、浓硫酸敞口放置后质量分数都会变小,是因为它们都有挥发性 |
分析 A、根据明矾净水原理是铝离子水解生成胶体,二氧化氯净水原理是杀菌消毒进行分析;
B、分子是保持物质化学性质的最小微粒,不同种分子性质不同;
C、根据氢氧化钠不能与水反应判断;
D、根据浓硫酸具有吸水性,不具有挥发性进行分析.
解答 解:A、明矾净水原理是明矾中的铝离子溶于水发生水解生成氢氧化铝胶体,胶体具有吸附性,能吸附水中悬浮杂质,二氧化氯净水原理是杀菌消毒,两者净水原理不同,故推理错误;
B、CO和CO2的化学性质不同,是因为它们分子的构成不同,不同种的分子性质不同,故推理正确.
C、氧化钙与水发生反应能放出大量热,但氢氧化钠是溶于水放热,不是与水反应,故推理错误;
D、浓盐酸具有挥发性,敞口放置后溶质氯化氢挥发,故溶质质量分数变小;浓硫酸具有吸水性,敞口放置后吸收水分,溶质质量分数减小,故推理错误.
故选:B.
点评 此题难度不大,掌握明矾和二氧化氯净水的原理、分子的性质和常见物质的性质等并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
11.近年来,我国多地出现雾霾天气.下列不属于大气污染物的是( )
| A. | PM2.5 | B. | SO2 | C. | NO2 | D. | CO2 |
12.2016年诺贝尔化学奖授予了在“分子机器”的设计和合成方面作出了杰出贡献的科学家.下列物质中,由分子构成的是( )
| A. | 金刚石 | B. | 氢气 | C. | 铁 | D. | 硫酸铜 |
9.下列各生活现象中,涉及化学变化的是( )
| A. | 粗盐潮解 | B. | 水果腐烂 | C. | 蔗糖溶解 | D. | 酒精挥发 |
16.某河道两旁有甲乙两厂.它们排放的污水各含有下列离子H+、Cu2+、K+、NO3-、OH-中的三种离子(两厂只含有一种相同的离子).若将两厂的污水按一定比例混合,沉淀后污水会变成无色澄清的中性溶液.下列关于污水的分析,不正确的是( )
| A. | Cu2+和OH-不可能来自同一工厂 | B. | Cu2+和 K+可能来自同一工厂 | ||
| C. | H+和OH-不可能来自同一工厂 | D. | NO3-和OH- 可能来自同一工厂 |
6.高铁酸钾(K2FeO4)具有高效的消毒作用,是一种新型非氯高效消毒剂,主要用于饮水处理.高铁酸钾中铁元素的化合价为( )
| A. | +2 | B. | +3 | C. | +6 | D. | +4 |
13.把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是( )
| A. | 蔗糖 | B. | 泥土 | C. | 汽油 | D. | 碘 |
10.在pH=1的无色溶液中能大量共存的离子组是( )
| A. | NH4+、Al3+、K+、Cl- | B. | Ba2+、K+、S2O32-、NO3- | ||
| C. | Al3+、Fe3+、SO42-、Cl- | D. | Na+、AlO2-、SO42-、NH4+ |
20.将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸质量增加而发生变化,如图所示.有关叙述中错误的是( )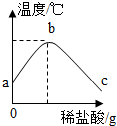

| A. | 从a到b过程中,烧杯中溶液的pH逐渐减小 | |
| B. | b点表示氢氧化钠和盐酸恰好完全反应 | |
| C. | c点表示所得溶液中溶质只有NaCl | |
| D. | 稀盐酸与氢氧化钠溶液发生的反应是放热反应 |