题目内容
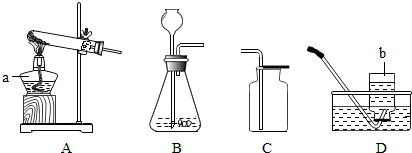
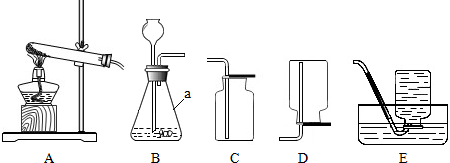
实验室用蔗糖配制50.0g溶质的质量分数为10%的蔗糖溶液,下列说法正确的是( )
| A、用托盘天平称取5.0g蔗糖 |
| B、用量程为10mL的量筒量取所需的水 |
| C、溶解蔗糖时,使用的玻璃仪器有烧杯、玻璃棒 |
| D、将配制好的溶液装入广口瓶中,塞好瓶塞并贴上标签 |
考点:一定溶质质量分数的溶液的配制
专题:溶液、浊液与溶解度
分析:根据已有的溶液配制的知识进行分析解答即可.
解答:解:A、50.0g溶质的质量分数为10%的蔗糖溶液,溶质质量为:50.0g×10%=5g,用托盘天平称取5.0g蔗糖,正确;
B、需要水的质量为50.0g-5g=45g,就是45mL,需要用量程为50mL的量筒量取,错误;
C、溶解蔗糖时,使用的玻璃仪器有烧杯、玻璃棒,正确;
D、将配制好的溶液装入细口瓶中,塞好瓶塞并贴上标签,错误;
故选AC.
B、需要水的质量为50.0g-5g=45g,就是45mL,需要用量程为50mL的量筒量取,错误;
C、溶解蔗糖时,使用的玻璃仪器有烧杯、玻璃棒,正确;
D、将配制好的溶液装入细口瓶中,塞好瓶塞并贴上标签,错误;
故选AC.
点评:本题考查了溶液配制的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
下列物质中均属于纯净物的是( )
| A、部分结冰的冰水混合物 硫磺 |
| B、洁净的空气 水泥沙浆混合土 |
| C、空气中分离出来的稀有气体 糖水 |
| D、加热高锰酸钾完全反应后的剩余固体物 酱油 |
下列有关溶液的计算说法不正确的是( )
| A、在某温度下,将35g KCl溶液蒸干得到7gKCl固体,则原溶液溶质质量分数为20% |
| B、把100g 98%浓硫酸稀释至10%稀硫酸,外加水的质量为880g |
| C、把50g10% NaCl溶液变为20%的NaCl溶液,需蒸发掉25g水 |
| D、在20℃时将40g KNO3充分溶解在100g水中,仍然有8.4g KNO3不溶.所得溶液中KNO3质量分数是31.6% |
下列说法不正确的是( )
| A、实验室里常用稀盐酸与大理石反应来制取少量二氧化碳气体 |
| B、“电解水实验”表明水是由氢元素和氧元素组成的 |
| C、铁丝在空气中剧烈燃烧,火星四射,生成黄色固体,放出大量的热 |
| D、资料介绍,成年人缺钙易得软骨病,这里的“钙”是指钙元素 |
水是生命的基础,没有水就没有生命,下列有关水的说法正确的是( )
| A、水由两个氢元素和一个氧元素组成 |
| B、无色,无臭,清澈透明的水就是纯水 |
| C、通电分解水生成的氧气和氢气的体积比为1:2 |
| D、可以大量开采地下水以满足社会对水的需求 |