题目内容
1.根据所学知识并结合下列仪器,回答有关问题: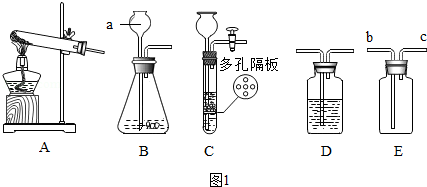
(1)写出图1中标有字母的仪器的名称:a长颈漏斗.
(2)实验室用A装置制取氧气,反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2 MnO4+MnO2+O2↑;如要制取并收集二氧化碳,可选用的装置组合是BE或CE,反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑,用D装置来检验二氧化碳,装置内发生的化学方程式是Ca(OH)2+CO2=CaCO3↓+H2O.
(3)实验室制取氢气的化学方程式是Zn+H2SO4═ZnSO4+H2↑,如果用如图1放置的E装置收集该气体,则气体从c端进入(填“b”或“c”);实验室常用装置C代替装置B制取氢气,该装置的优点是通过开关活塞来控制反应的开始和停止,图2和此装置原理相同的是ABD.
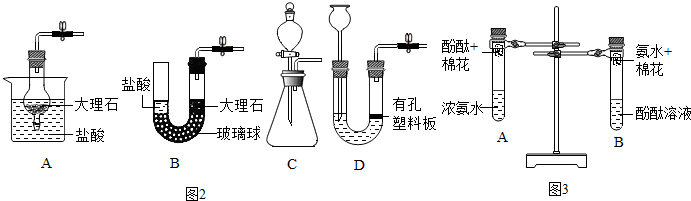
(4)在分子运动实验中,为帮助同学解决认识中的误区,爱实验的小赵改进了实验酚酞+棉花氨水+棉花浓氨水酚酞溶液AB装置,如图3所示:实验过程中能观察到A试管中的实验现象是棉花上的酚酞很快变红了,约4分钟后才会观察到B中现象,为能快速观察B中的现象,同学们提出用热毛巾捂住B试管,依据是温度升高,分子的运动速率变快.
分析 (1)熟悉常见仪器,根据仪器的形状和用途判断名称;
(2)根据发生装置的特点可判断反应物状态和反应条件;根据收集装置可判断气体的性质,综合后可判断制取的气体;熟记实验室制取二氧化碳的化学反应式;
(3)实验室制取氢气常采用锌和稀硫酸来制取氢气,锌和稀硫酸在常温下反应生成硫酸锌和氢气;氢气的密度比空气小,能溶于水;分液漏斗可控制反应的发生于停止;
(4)浓氨水具有挥发性.浓氨水中的氨气分子运动的快.酚酞溶液中酚酞运动慢,A试管中的棉花先变红;
解答 解:(1)实验仪器a的名称是长颈漏斗;
(2)高锰酸钾在加热的条件下,生成锰酸钾和二氧化锰和氧气,或氯酸钾和二氧化锰做催化剂,在加热的条件下生成氯化钾和氧气,配平即可.故答案为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2 MnO4+MnO2+O2↑;实验室用大理石与稀盐酸制取二氧化碳,二氧化碳的密度大于空气的密度,二氧化碳能溶于水,所以只能用向上排空气法收集,.
反应原理用化学方程式表示是 CaCO3+2HCl═CaCl2+H2O+CO2↑;氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水;反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
(3)实验室制取氢气常采用锌和稀硫酸来制取氢气,锌和稀硫酸在常温下反应生成硫酸锌和氢气,反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑.氢气的密度比空气小,如果用如图1放置的E装置收集该气体,则气体从c端进入;实验室常用装置C代替装置B制取氢气,该装置的优点是通过开关活塞来控制反应的开始和停止,图2和此装置原理相同的是ABD;
(4)浓氨水具有挥发性.是由于浓氨水中的氨气分子运动的快.酚酞溶液中酚酞运动慢,A试管中的棉花先变红;为能快速观察B中的现象,同学们提出用热毛巾捂住B试管,依据是温度升高,分子的运动速率变快.
故答案为:(1)长颈漏斗;(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2 MnO4+MnO2+O2↑、BE或CE、CaCO3+2HCl═CaCl2+H2O+CO2↑、Ca(OH)2+CO2=CaCO3↓+H2O;
(3)Zn+H2SO4=Zn SO4+H2↑,C,ABD;
(4)棉花上的酚酞很快变红了、温度升高,分子的运动速率变快.
点评 实验装置的选取要看反应物的状态和反应条件,收集装置的选取要看气体的密度和溶水性,这些是实验和考题中的常见问题,同学们一定要记清.

| A. | O2 | B. | CO2 | C. | SO2 | D. | N2 |
| A. | CO32- | B. | NO3- | C. | SO42- | D. | K+ |
| A. | 密度比空气大 | B. | 不易燃烧 | C. | 易分解 | D. | 不易导电 |
| A. | 向试管里倾倒液体时,试剂瓶口要紧挨试管口 | |
| B. | 用滴管滴加液体时,滴管不能触及容器的内壁 | |
| C. | 为节约火柴,用燃着的酒精灯引燃其他酒精灯 | |
| D. | 用量筒量取液体时,视线要与量筒内液体的凹液面的最低处保持水平 |
| A. | 物质溶解往往伴随有能量的变化 | |
| B. | 铝比铁具有更好的抗腐蚀性能,是因为铁比铝更活泼 | |
| C. | 建造游泳中心“水立方”用到的聚乙烯是有机合成材料 | |
| D. | 用汽油和加了洗涤剂的水分别除去衣服上的油污,两者去污原理不同 |
| A. | 用食醋除去暖水瓶中的水垢 | |
| B. | 用燃烧的方法鉴别衣料中的羊毛纤维 | |
| C. | 油锅着火时可以立即盖上锅盖 | |
| D. | 碳铵与草木灰混合可以提高肥效 |
| A. | 液氧 | B. | 氨水 | C. | 不锈钢 | D. | 矿泉水 |
 取盐酸与氯化铜的混合溶液27g放入烧杯中,逐滴滴入质量分数为20%的氢氧化钠溶液,产生沉淀质量与滴入氢氧化钠溶液质量关系如图所示.
取盐酸与氯化铜的混合溶液27g放入烧杯中,逐滴滴入质量分数为20%的氢氧化钠溶液,产生沉淀质量与滴入氢氧化钠溶液质量关系如图所示.