题目内容
9. 取盐酸与氯化铜的混合溶液27g放入烧杯中,逐滴滴入质量分数为20%的氢氧化钠溶液,产生沉淀质量与滴入氢氧化钠溶液质量关系如图所示.
取盐酸与氯化铜的混合溶液27g放入烧杯中,逐滴滴入质量分数为20%的氢氧化钠溶液,产生沉淀质量与滴入氢氧化钠溶液质量关系如图所示.(1)氢氧化钠溶液的质量在0-4g时,发生反应的化学方程式为HCl+NaOH=NaCl+H2O.
(2)与氯化铜反应的氢氧化钠的质量为1.6g.
(3)原盐酸与氯化铜的混合溶液中氯化铜的质量分数(写出计算过程).
分析 (1)根据图象可以看出,滴入NaOH溶液的质量在0~4g时,没有出现沉淀,所以是盐酸和氢氧化钠的反应,盐酸和氢氧化钠反应生成氯化钠和水进行分析;
(2)根据图象中的数据可以看出,从加入氢氧化钠4g开始出现沉淀,到加入氢氧化钠12g,沉淀开始不变进行分析;
(3)根据氢氧化钠和氯化铜反应生成氢氧化铜沉淀和氯化钠,结合题中所给的数据进行分析.
解答 解:(1)从图象可以看出,滴入NaOH溶液的质量在0~4g时,没有出现沉淀,所以是盐酸和氢氧化钠的反应,盐酸和氢氧化钠反应生成氯化钠和水,化学方程式为:HCl+NaOH=NaCl+H2O;
(2)从图象中的数据可以看出,从加入氢氧化钠4g开始出现沉淀,到加入氢氧化钠12g,沉淀开始不变,所以与氯化铜反应的NaOH的质量:(12-4)g×20%=1.6g;
(3)设原盐酸与氯化铜的混合溶液中氯化铜的质量为x,
CuCl2+2NaOH=Cu(OH)2↓+2NaCl
135 80
x 8g×20%
则$\frac{135}{80}=\frac{x}{5g×20%}$,解得x=2.7g.
所以原盐酸与氯化铜的混合溶液中氯化铜的质量分数为:$\frac{2.7g}{27g}$×100%=10%.
故答案为:
(1)HCl+NaOH=NaCl+H2O;(2)1.6;(3)10%.
点评 本题重点考查复分解反应的实质,学会分析图象,判断产物,属于一道溶液综合性的题目.本题是溶液和化学反应、图象融合的题目,是综合性的题型,要求比较高.解答本题的关键是根据图象分析出生成的氢氧化铜的质量.

练习册系列答案
相关题目
19.下列变化中,属于化学变化的是( )
| A. |  对干燥的玻璃片哈气 | B. |  用合金在纯金属上刻画 | ||
| C. |  燃放礼花 | D. |  活性碳吸附毒气 |
20.下列是人体中几种液体的正常pH范围,其中酸性最强的是( )
| A. | 胃液(0.9-1.5) | B. | 血浆(7.35-7.45) | C. | 尿液(4.7-8.4) | D. | 胰液(7.5-8.0) |
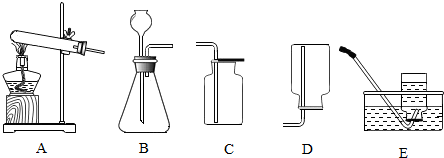
17. 如图为某同学制作的用浓硫酸催化甲酸(HCOOH)制取CO还原氧化铜的微型实验装置,下列说法不正确的是( )
如图为某同学制作的用浓硫酸催化甲酸(HCOOH)制取CO还原氧化铜的微型实验装置,下列说法不正确的是( )
 如图为某同学制作的用浓硫酸催化甲酸(HCOOH)制取CO还原氧化铜的微型实验装置,下列说法不正确的是( )
如图为某同学制作的用浓硫酸催化甲酸(HCOOH)制取CO还原氧化铜的微型实验装置,下列说法不正确的是( )| A. | Y型管中发生的反应为:HCOOH$\frac{\underline{\;浓H_{2}SO_{4}\;}}{△}$H2O+CO↑ | |
| B. | 观察到的现象是氧化铜变成了铜,且澄清石灰水变浑浊 | |
| C. | 此实验装置的主要优点尾气处理有效节能 | |
| D. | 眼药水瓶可改用注射器代替 |
14.化学与人类进步和社会发展的关系非常密切,下列说法不合理的是( )
| A. | 有计划、合理地开采矿物,并利用新技术寻找金属的代用品,以保护金属资源 | |
| B. | 推广使用车用乙醇汽油,可适当节省石油资源,并有效上地减少汽车尾气污染 | |
| C. | 将污水经物理、化学等方法进行分级处理后可达到农灌或绿化用水标准 | |
| D. | 塑料制品的成本低,而且耐用、防水,应大力提倡使用 |
18.X、R表示两种金属,在溶液中发生反应:X+3RNO3═3R+X(NO3)3.下列说法不正确的是( )
| A. | X可能是Fe,R可能是Cu | |
| B. | 若X是Al,R是Ag,则反应后溶液质量减少 | |
| C. | 该反应是置换反应 | |
| D. | X的金属活动性比R强 |