题目内容
12.某溶液中大量存在的离子仅有NH4+、Ba2+和X离子,则X可能是( )| A. | CO32- | B. | NO3- | C. | SO42- | D. | K+ |
分析 根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能共存,据此进行分析判断即可.
解答 解:A、Ba2+、CO32-两种离子能结合成碳酸钡沉淀,不能大量共存,故选项错误.
B、NO3-和NH4+、Ca2+不能结合成沉淀、气体或水,能大量共存,故选项正确.
C、Ba2+、SO42-两种离子能结合成硫酸沉淀,不能大量共存,故选项错误.
D、某溶液中大量存在的离子仅有NH4+、Ca2+和X离子,NH4+、Ca2+均带正电荷;溶液中应含有阳离子和阴离子,K+也带正电荷,不符合要求,故选项错误.
故选:B.
点评 本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水.

练习册系列答案
相关题目
2.下列选项中,实验操作一定能够达到相对于实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 除去CO中的少量H2O和CO2 | 先通过浓硫酸,再通过氢氧化钠溶液 |
| B | 验证Al、Cu、Ag的金属活动性 | 将Al丝分别浸入CuSO4溶液、AgNO3溶液 |
| C | 探究NaOH固体是否变质 | 取少量固体,加水溶解,滴加足量稀盐酸,观察是否有气泡产生 |
| D | 鉴别:①CuSO4溶液②稀硫酸③NaCl溶液④NaOH溶液 | 不再使用其他任何试剂就能鉴别,且鉴别出的顺序为①④②③或①④③② |
| A. | A | B. | B | C. | C | D. | D |
20.下列是人体中几种液体的正常pH范围,其中酸性最强的是( )
| A. | 胃液(0.9-1.5) | B. | 血浆(7.35-7.45) | C. | 尿液(4.7-8.4) | D. | 胰液(7.5-8.0) |
7.为了验证金属的活动性,同学们将洁净的铁钉放入硫酸铜溶液中,观察到铁钉表面变为红色,反应的化学方程式为Fe+CuSO4═FeSO4+Cu.细心的同学发现,铁钉表面同时含有气泡冒出,就此气泡成分,同学们在老师指导下进行了如下探究:
【提出猜想】
同学们一致认为C同学的猜想是不合理的,理由是根据质量守恒定律,化学反应前后元素种类不变,反应物中没有碳元素所以生成物中一定没有二氧化碳.
【查阅资料】二氧化硫具有漂白性,会使品红溶液褪色.
【进行实验】利用如图所示的装置分别进行实验
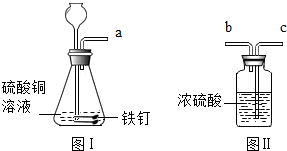
(1)反应一段时间后,A同学将带火星的木条放在a处,观察到带火星的木条没有复燃,则她的猜想错误.
(2)B同学将产生的气体通入品红溶液中,观察到品红溶液不褪色,则她的猜想也错误.
(3)D同学将图Ⅰ中的a端导管与图Ⅱ中的c端导管相连,目的是对其他进行干燥.反应一段时间后,点燃从图Ⅱ另一端导管出来的气体,通过对现象的分析,得出他的猜想正确.
【得出结论】铁与硫酸铜溶液反应时伴随产生了氢气.
【讨论反思】这几位同学的实验方案存在安全隐患,理由是该实验中氢气属于可燃性气体,不纯点燃可能会发生爆炸,改进的方法是先将从a处的气体通入图Ⅱ一段时间后再点燃.
【继续追问】铁与硫酸铜溶液反应为什么会伴随产生氢气?
【查阅资料】有些盐在水溶液中会发生水解反应,使盐溶液不一定呈中性.
【再次猜想】硫酸铜溶液可能显酸性.
【验证方案】
【反思与评价】同学们做完以上实验很有成就感,体验到探究的快乐,并感慨“科学探究无止境”!
【提出猜想】
| 同学 | A | B | C | D |
| 对气泡成分的猜想 | 氧气 | 二氧化硫 | 二氧化碳 | 氢气 |
【查阅资料】二氧化硫具有漂白性,会使品红溶液褪色.
【进行实验】利用如图所示的装置分别进行实验

(1)反应一段时间后,A同学将带火星的木条放在a处,观察到带火星的木条没有复燃,则她的猜想错误.
(2)B同学将产生的气体通入品红溶液中,观察到品红溶液不褪色,则她的猜想也错误.
(3)D同学将图Ⅰ中的a端导管与图Ⅱ中的c端导管相连,目的是对其他进行干燥.反应一段时间后,点燃从图Ⅱ另一端导管出来的气体,通过对现象的分析,得出他的猜想正确.
【得出结论】铁与硫酸铜溶液反应时伴随产生了氢气.
【讨论反思】这几位同学的实验方案存在安全隐患,理由是该实验中氢气属于可燃性气体,不纯点燃可能会发生爆炸,改进的方法是先将从a处的气体通入图Ⅱ一段时间后再点燃.
【继续追问】铁与硫酸铜溶液反应为什么会伴随产生氢气?
【查阅资料】有些盐在水溶液中会发生水解反应,使盐溶液不一定呈中性.
【再次猜想】硫酸铜溶液可能显酸性.
【验证方案】
| 操作 | 现象 | 结论 |
| 向硫酸铜溶液中滴加石蕊试液 | 溶液变红 | [再次猜想]是正确的. |
17. 如图为某同学制作的用浓硫酸催化甲酸(HCOOH)制取CO还原氧化铜的微型实验装置,下列说法不正确的是( )
如图为某同学制作的用浓硫酸催化甲酸(HCOOH)制取CO还原氧化铜的微型实验装置,下列说法不正确的是( )
 如图为某同学制作的用浓硫酸催化甲酸(HCOOH)制取CO还原氧化铜的微型实验装置,下列说法不正确的是( )
如图为某同学制作的用浓硫酸催化甲酸(HCOOH)制取CO还原氧化铜的微型实验装置,下列说法不正确的是( )| A. | Y型管中发生的反应为:HCOOH$\frac{\underline{\;浓H_{2}SO_{4}\;}}{△}$H2O+CO↑ | |
| B. | 观察到的现象是氧化铜变成了铜,且澄清石灰水变浑浊 | |
| C. | 此实验装置的主要优点尾气处理有效节能 | |
| D. | 眼药水瓶可改用注射器代替 |
2.下列物品所含的主要材料,不属于合成材料的是( )
| A. | 涤纶衣 | B. | 塑料杯 | C. | 蚕丝被 | D. | 汽车轮胎 |