题目内容
某化验员为测定长期暴露在空气里的苛性钠的纯度,他先将w g这种苛性钠配成溶液,加入几滴酚酞试液,溶液呈红色;再逐滴加入m g a%的稀硫酸溶液,溶液恰恰由红色变成无色,同时收集到n g二氧化碳.据此这种苛性钠纯度的计算式为 .
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据收集到n克二氧化碳气体的质量可以求出碳酸钠的质量.再根据碳酸钠的质量可以求出样品中氢氧化钠的质量,进而求出苛性钠样品中的NaOH的质量分数.
解答:解:设苛性钠样品中Na2CO3的质量为X
H2 SO4+Na2CO3═Na2SO4+H2O+CO2↑
106 44
x ng
=
x=
g
苛性钠样品中的NaOH质量分数
×100%=1-
答:苛性钠样品中的NaOH质量分数为1-
.
H2 SO4+Na2CO3═Na2SO4+H2O+CO2↑
106 44
x ng
| 106 |
| x |
| 44 |
| ng |
x=
| 53n |
| 22 |
苛性钠样品中的NaOH质量分数
(w-
| ||
| wg |
| 53n |
| 22w |
答:苛性钠样品中的NaOH质量分数为1-
| 53n |
| 22w |
点评:此题属于多步计算题,需正确写出方程式,再准确找出各物质之间的质量关系,才可以解出.此类题由于步骤繁琐,在中考中已不多见.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
饮用清天然矿泉水对人体健康有益,原因之一是矿泉水的pH与人体血液的pH相似.已知某种矿泉水的pH为7.2-7.5,该矿泉水的酸碱性为( )
| A、强酸性 | B、强碱性 |
| C、弱酸性 | D、弱碱性 |
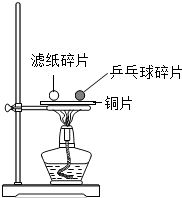 某兴趣小组围绕“燃烧条件”这一主题开展如下探究活动,请你参与:
某兴趣小组围绕“燃烧条件”这一主题开展如下探究活动,请你参与: