题目内容
如图是钠元素、氧元素在周期表中的相关信息及有关粒子的结构示意图.下列说法错误的是( )


| A、钠元素的原子序数为11 |
| B、氧离子的结构示意图是D |
| C、AB两种元素组成的化合物的化学式可为Na2O |
| D、钠元素与氧元素的最本质的区别是最外层电子数不同 |
考点:元素周期表的特点及其应用,原子结构示意图与离子结构示意图
专题:化学用语和质量守恒定律
分析:由钠元素、氧元素在周期表中的相关信息及有关粒子的结构示意图可知:钠元素的原子序数、元素的最本质的区别、最外层电子数等信息;掌握元素的概念:具有相同的质子数的一类原子的总称.
A、由钠元素在周期表中的相关信息可知,钠元素的原子序数;
B、根据原子得失电子规律,由氧原子的原子结构示意图可推测其离子的结构示意图;
C、AB两种元素分别为钠元素和氧元素,根据它们得失电子情况,判断其组成的化合物的化学式;
D、掌握元素的概念:具有相同的质子数的一类原子的总称;质子数不同,则元素种类不同.
A、由钠元素在周期表中的相关信息可知,钠元素的原子序数;
B、根据原子得失电子规律,由氧原子的原子结构示意图可推测其离子的结构示意图;
C、AB两种元素分别为钠元素和氧元素,根据它们得失电子情况,判断其组成的化合物的化学式;
D、掌握元素的概念:具有相同的质子数的一类原子的总称;质子数不同,则元素种类不同.
解答:解:A、由钠元素在周期表中的相关信息可知,钠元素的原子序数为11,故A正确;
B、氧原子的结构示意图是C,它最外层电子数为6,易得2个电子,故氧离子的结构示意图是D,故B正确;
C、AB两种元素在形成化合物时,A易失去1个电子,B易得2个电子,所以组成的化合物的化学式为Na2O,故C正确;
D、钠元素与氧元素的最本质的区别是核内质子数不同,而非故最外层电子数不同,故D错误.
故选D.
B、氧原子的结构示意图是C,它最外层电子数为6,易得2个电子,故氧离子的结构示意图是D,故B正确;
C、AB两种元素在形成化合物时,A易失去1个电子,B易得2个电子,所以组成的化合物的化学式为Na2O,故C正确;
D、钠元素与氧元素的最本质的区别是核内质子数不同,而非故最外层电子数不同,故D错误.
故选D.
点评:了解原子结构示意图与离子结构示意图的区别和联系;掌握核外电子在化学变化中的作用和得失电子的规律特点;掌握元素的概念;了解元素周期表的特点及其应用.

练习册系列答案
相关题目
用“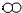 ”和“
”和“ ”代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的模拟模型如图所示,下列说法正确的是( )
”代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的模拟模型如图所示,下列说法正确的是( )
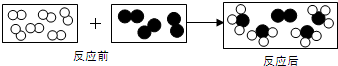
 ”和“
”和“ ”代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的模拟模型如图所示,下列说法正确的是( )
”代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的模拟模型如图所示,下列说法正确的是( )
A、参加反应的“ ”和“ ”和“ ”分子的个数比是 2:1 ”分子的个数比是 2:1 |
| B、该反应是化合反应 |
| C、该反应有2种生成物 |
| D、该反应不遵循质量守恒定律 |
 现在的社会对能量需求会很大,人类通过化学反应获得的能量大多来自于化石燃料,开发和使用新能源上进行了很多尝试,比如街头路灯,每天只要短时间光照就能使用(如图),这种新能源是( )
现在的社会对能量需求会很大,人类通过化学反应获得的能量大多来自于化石燃料,开发和使用新能源上进行了很多尝试,比如街头路灯,每天只要短时间光照就能使用(如图),这种新能源是( )| A、太阳能 | B、风能 | C、核能 | D、氢能 |
下列属于中和反应的是( )
| A、CuSO4+2NaOH═Cu(OH)2↓+Na2SO4 |
| B、AgNO3+HCl═AgCl↓+HNO3 |
| C、CaCO3+2HCl═CaCl2+H2O+CO2↑ |
| D、H2SO4+2NaOH═Na2SO4+2H2O |
下列实验基本操作正确的是( )
A、 蒸发食盐水 |
B、 放入块状固体 |
C、 稀释浓硫酸 |
D、 过滤 |
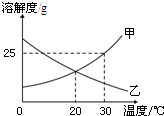 甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )| A、甲物质的溶解度比乙物质的溶解度大 |
| B、升温能使甲物质的不饱和溶液变为饱和溶液 |
| C、20℃时,两种物质的饱和溶液中溶质的质量分数相等 |
| D、30℃时,100g甲的饱和溶液中含有25g甲物质 |
下列各物质中含分子数最多的是( )
| A、0.1mol HCl |
| B、3.01×1023个I2 |
| C、1mol F2 |
| D、0.05mol Br2 |
 如图为硝酸钾和氯化钠的溶解度曲线.由图可知:
如图为硝酸钾和氯化钠的溶解度曲线.由图可知: