题目内容
1. 如图是电解水的实验装置,通电后,两电极上都有气体放出,该实验加入稀硫酸的目的是增强水的导电性,试管A、B中两气体的质量比约为1:8.
如图是电解水的实验装置,通电后,两电极上都有气体放出,该实验加入稀硫酸的目的是增强水的导电性,试管A、B中两气体的质量比约为1:8.
分析 水电解实验要向水中加入一些稀硫酸,增强水的导电性,负极生成氢气,正极生成氧气,二者的体积比是2:1,质量比是1;8.
解答 解:水电解实验要向水中加入一些稀硫酸,增强水的导电性,负极生成氢气,正极生成氧气,二者的体积比是2:1,由此可断定A为氢气,B为氧气,根据反应前后元素的质量不变,所以生成氢气和氧气的质量比等于水中氢、氧元素的质量比:(1×2):16=1:8.
故答案为:增强水的导电性;1:8.
点评 本题难度不大,掌握电解水的实验现象、结论(正氧负氢,氢二氧一),难度不大.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
11.有三瓶失去标签的无色溶液,只知道它们分别是NaOH、NaCl、BaCl2中的各一种.下列四种溶液中,能将三种无色溶液一次鉴别出来的是( )
| A. | 硫酸铜溶液 | B. | 酚酞试液 | C. | 硝酸银溶液 | D. | 稀硫酸 |
12.将镁和铁的混合物8.4g投入足量的稀硫酸中充分反应,产生氢气的质量可能为( )
| A. | 0.3g | B. | 0.5g | C. | 0.7g | D. | 1.2g |
6.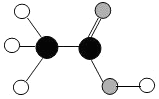 食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中
食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中 代表一个碳原子,
代表一个碳原子, 代表一个氢原子,
代表一个氢原子, 代表一个氧原子.下列说法正确的是( )
代表一个氧原子.下列说法正确的是( )
 食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中
食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中 代表一个碳原子,
代表一个碳原子, 代表一个氢原子,
代表一个氢原子, 代表一个氧原子.下列说法正确的是( )
代表一个氧原子.下列说法正确的是( )| A. | 乙酸是一种化合物 | |
| B. | 乙酸的相对分子质量为60 | |
| C. | 乙酸中碳元素的质量分数最大 | |
| D. | 乙酸分子中的碳原子、氢原子、氧原子的个数比为1:2:1 |
13.“低碳生活”是指在生活作息时减少能量耗用,使二氧化碳排放降低的一种时尚生活方式,下列不符合“低碳生活”主题的是( )
| A. | 深秋时节焚烧落叶 | B. | 参加“地球熄灯一小时”活动 | ||
| C. | 开发回收利用二氧化碳的新技术 | D. | 用旧报纸制铅笔杆 |
10.通过实验进行证据推断是学习化学的重要方法,下列图示实验得出的结论正确的是( )


| A. | 图1所示实验既说明甲烷具有可燃性,有水生成又说明甲烷中含有氧元素 | |
| B. | 图2所示实验既说明CO2密度比空气大,又说明CO2不能燃烧也不支持燃烧 | |
| C. | 图3所示实验既说明电解水生成氢气和氧气,又说明水是由氢气和氧气组成的 | |
| D. | 图4所示实验既可探究可燃物的燃烧条件,又说明红磷不是可燃物 |
