题目内容
3.某兴趣小组对中和反应进行如下实验探究:
【探究实验一】借助无色酚酞试剂,证明酸碱发生了反应.
甲同学按图1进行实验,证明了盐酸和NaOH溶液能发生化学反应,他依据的实验现象是红色变无色,写出该反应的化学方程式NaOH+HCl=NaCl+H2O.
【探究实验二】检验反应生成的水,证明酸碱发生了反应.
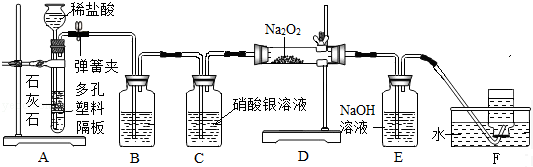
乙同学取硅胶(一种不与酸、碱反应的干燥剂,吸水后由蓝色变红色)、无水醋酸(一种酸,
常温下为液体)和固体氢氧化钠进行图2所示的三个实验.
①实验A和B可以作为参照,其目的是证明无水醋酸和氢氧化钠固体中不含水;
②加入试剂后迅速塞紧橡胶塞的原因是防止空气中的水蒸气进入试管;
③能证明酸和碱反应有水生成的现象是硅胶由蓝色变红色.
④实验C中发生反应的化学方程式为:CH3COOH+NaOH→CH3COONa+H2O,中和0.05mol的无水醋酸(化学式为CH3COOH)需要2g氢氧化钠固体(根据化学方程式列式计算).
分析 【探究活动一】根据酚酞在酸、碱溶液中的颜色的变化分析;
【探究活动二】
①根据硅胶的颜色的变化分析反应是否有有水生成;
②根据空气的成分分析;
③通过实验对比,硅胶颜色的变化分析;
解答 解:【探究活动一】无色酚酞试液在氢氧化钠溶液中显红色,滴入了稀盐酸变成了无色,说明了盐酸与氢氧化钠发生了反应;该反应的化学方程式为:NaOH+HCl=NaCl+H2O;
【探究活动二】
①通过实验A、B的实验现象的对比证明了无水醋酸和氢氧化钠不含有水,不能使硅胶变色,由试验③硅胶的变色说明了中和反应有水生成.
②空气中含有水,也能使硅胶变色,迅速塞紧橡胶塞可防止空气中的水分进入试管干扰试验;
③能证明酸和碱反应有水生成的现象是:实验AB对比,C硅胶颜色的变化;
④设需要氢氧化钠的物质的量为xmol,
CH3COOH+NaOH═CH3COONa+H2O
1 1
0.05mol x
$\frac{1}{0.05mol}=\frac{1}{x}$
x=0.05mol
氢氧化钠固体的质量=0.05mol×40g/mol=2g
故答案为:
【探究活动一】红色变无色;NaOH+HCl=NaCl+H2O;
【探究活动二】
①证明无水醋酸和氢氧化钠固体中不含水;
②防止空气中的水蒸气进入试管;
③硅胶由蓝色变红色;
④2
点评 本题属于实验探究题,综合性较强,既有试验探究,又有实验数据图象的分析.只有综合掌握了基础知识才能较好的完成本类练习题.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案
相关题目
13.水是我们身边重要的物质,下列说法不正确的是( )
| A. | 可用肥皂水区别硬水和软水 | |
| B. | H2O是由一个氢分子和一个氧原子构成 | |
| C. | H2O中氧元素的化合价为-2 | |
| D. | H2O是氧化物 |
18.书写错误的化学式为( )
| A. | 氦气:He | B. | 氧化铁:FeO | C. | 氢氧化钾:KOH | D. | 碳酸:H2CO3 |
8.下列除去杂质所用的药品或方法,不正确的是( )
| 选项 | 物质 | 杂质 | 除杂药品或方法 |
| A | NaCl溶液 | Na2SO4 | 加入过量的BaCl2溶液,过滤 |
| B | CaO | CaCO3 | 高温煅烧至质量不再改变 |
| C | N2 | O2 | 灼热的铜网 |
| D | NaCl | KNO3 | 溶解、降温结晶、过滤 |
| A. | A | B. | B | C. | C | D. | D |
15.如图图象与操作相对应,其中合理的是( )
| A. | 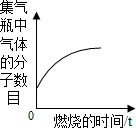 少量的硫磺在密闭的集气瓶中与氧气完全燃烧 | |
| B. | 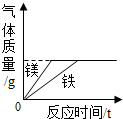 常温下,少量等质量的镁、铁分别同时放入足量等质量、等质量分数的稀盐酸中 | |
| C. | 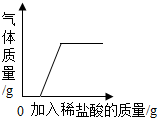 向部分变质的NaOH溶液中滴加过量稀盐酸 | |
| D. | 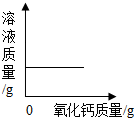 一定温度时,向一定量饱和石灰水中加入氧化钙 |