题目内容
11.我们周围的物质世界是由100多种元素组成的,为了便于研究元素的性质,常常需要寻找它们之间的内在规律.下表列出的是1~18号元素的部分最高正化合价和最低负化合价.请你阅读后,回答下列问题: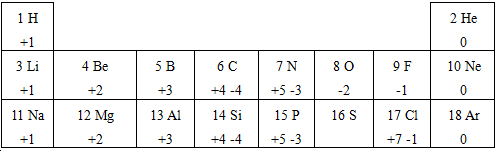
(1)很多科学家对元素周期表的发现和完善做出了重大贡献,请写出其中一位科学家的名字门捷列夫.
(2)表中不同种元素最本质的区别是A(填序号).
A.质子数不同 B.中子数不同
C.相对原子质量不同 D.电子数不同
(3)11号元素属于金属元素(填“金属”或“非金属”),它在化学反应中形成的粒
子与Ne(写元素符号)原子具有相同的核外电子排布.
(4)16号元素的原子核外电子数为16,推测该元素最低负化合价为-2,最高正化
合价的氧化物的化学式为SO3.
(5)从化合价角度分析,我们可以发现一些规律.请写出其中的一个:同一横行(周期)从左到右元素的正化合价逐渐升高.
(6)某元素R与硫酸根形成化合物的化学式为:RSO4,其相对分子质量为152,回答下列问题:
①R的元素符号为Fe.
②R在化合物中可以显+3价,则+3价R的氧化物的化学式为Fe2O3,+3价R的氧化物中R的质量分数是多少?(写出计算过程)
分析 (1)根据1869年以门捷列夫为代表的科学家发现了元素周期表,进行解答;
(2)根据不同种元素最本质的区别是质子数不同;进行解答;
(3)根据11号元素的信息确定元素的分类,进而确定在化学反应中形成的粒子的核外电子排布.
(4)根据原子序数在数值上等于核电荷数,在原子中:核电荷数=质子数=电子数等进行分析解答.
(5)根据表格提供的信息可以看出,抓住化合价数据的共性从横向上、纵向上进行分析解答本题.
(6)依据相对分子质量求某种元素的相对原子质量,依据化合价写化学式,根据化学式求某种元素的质量分数.
解答 解:(1)根据1869年以门捷列夫为代表的科学家发现了元素周期表,因此元素周期表的发现,其中一位科学家的名字:门捷列夫;故答案为:门捷列夫;
(2)根据不同种元素最本质的区别是质子数不同; 故选A;
(3)11号元素是钠元素,属于金属元素,失去电子后,形成的钠离子核外带10个电子,与氖原子具有相同的核外电子排布;故答案为:金属;Ne;
(4)16号元素的原子序数为16,根据原子序数在数值上等于核电荷数,在原子中:核电荷数=质子数=电子数,则原子核外电子数为16;在化学反应中能得到两个电子,形成硫离子,带两个单位的负电荷,故最低负化合价为-2价;同一周期,从左向右,元素的最高正化合价依次增大,则16号元素最高正化合价应为+6,其最高正化合价的氧化物的化学式为 S03;故答案为:16;-2;S03;
(5)根据表格提供的信息可以看出,同一列元素具有相同的化合价;同一行(周期)从左到右元素的最高正化合价逐渐升高,故答案为:同一横行(周期)从左到右元素的正化合价逐渐升高;
(6)①设R的相对原子质量为X,则X+32+16×4=152,则X=56.故答案为Fe;
②因为R在化合物中可以显+3价,则+3价R的氧化物的化学式为:Fe2O3;Fe2O3中Fe的质量分数为:$\frac{56×2}{56×2+16×3}$×100%=70%,
故答案为:Fe2O3;70%.
点评 本题难度不是很大,考查了元素周期表的应用,掌握元素周期律及化学式计算、化合价的有关知识是正确解答本题的关键.

 学习完“酸、喊、盐的性质”后,老师将两瓶未贴标签的饱和石灰水、饱和碳酸钠溶液摆放在实验桌上,让同学们区分.下面是“雄鹰小组”同学们的探究过程:
学习完“酸、喊、盐的性质”后,老师将两瓶未贴标签的饱和石灰水、饱和碳酸钠溶液摆放在实验桌上,让同学们区分.下面是“雄鹰小组”同学们的探究过程: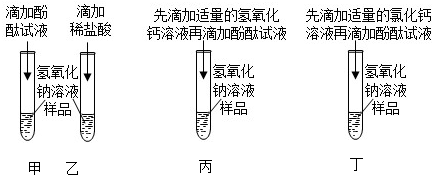
 碳与碳的化合物在工农业生产及日常生活中有广泛的用途.
碳与碳的化合物在工农业生产及日常生活中有广泛的用途. 如图为实验室制取二氧化碳的实验装置图,请回答下列问题:
如图为实验室制取二氧化碳的实验装置图,请回答下列问题: