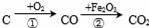题目内容
以下是实验室常用的部分仪器.
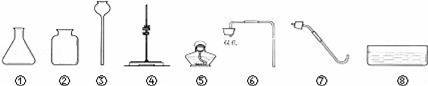

(1)仪器⑧的名称为 ;
(2)某同学要用过氧化氢溶液和二氧化锰混合制取氧气,已经选择了仪器①②③,则还需要从上图中选择的仪器是 (填一种仪器的序号);反应的化学方程式为 ;
(3)使用仪器③的目的是 ;
(4)该套装置还可用于实验室制取CO2,若用73g10%的稀盐酸与足量的大理石充分反应,能产生CO2的质量是 g.
【考点】氧气的制取装置;氧气的收集方法;书写化学方程式、文字表达式、电离方程式;根据化学反应方程式的计算.
【专题】化学用语和质量守恒定律;常见仪器及化学实验基本操作;常见气体的实验室制法、检验、干燥与净化;有关化学方程式的计算.
【分析】(1)据常用仪器回答;
(2)过氧化氢溶液和二氧化锰混合制取氧气属于固液常温型,该同学选择了仪器①②③,有长颈漏斗,则须选择双孔塞,并据反应原理书写方程式;
(3)长颈漏斗可随时添加液体药品;
(4)据溶质的质量=溶液的质量×溶质的质量分数可计算出稀盐酸中含有溶质的质量,并结合方程式计算出二氧化碳的质量.
【解答】解:(1)标号仪器是水槽;
(2)过氧化氢溶液和二氧化锰混合制取氧气属于固液常温型,该同学选择了仪器①②③,有长颈漏斗,则选择双孔塞,反应方程式是2H2O2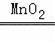
 2H2O+O2↑;
2H2O+O2↑;
(3)长颈漏斗可随时添加液体药品过氧化氢溶液;
(4)73g10%的稀盐酸中溶质的质量是73g×10%=7.3g;
设能产生CO2的质量是x
CaCO3+2HCl=CaCl2+CO2↑+H2O
73 44
7.3g x
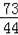
 =
=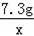

x=4.4g
故答案为:(1)水槽; (2)⑥;2H2O2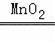
 2H2O+O2↑;(3)便于添加过氧化氢溶液; (4)4.4.
2H2O+O2↑;(3)便于添加过氧化氢溶液; (4)4.4.
【点评】掌握制取气体的反应原理、方程式计算的一般方法、常用仪器的名称和用途,及装置选取方法,即可结合题意正确解答.




 2SO2+2H2O
2SO2+2H2O
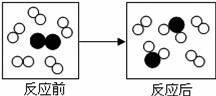
 ”表示氮原子,“
”表示氮原子,“
 ”表示氢原子.下列判断错误的是( )
”表示氢原子.下列判断错误的是( )