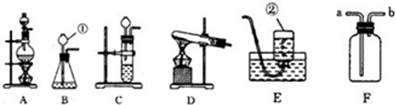
题目内容
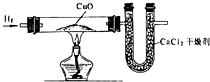 有人利用氢气还原氧化铜的实验来测定水的组成.如图得到下列结果:
有人利用氢气还原氧化铜的实验来测定水的组成.如图得到下列结果:| 实 验 | 实验前(g) | 实验后(g) |
| 氧化铜+玻璃管 | 72.8 | 66.4 |
| 氯化钙+U形管 | 102.9 | 110.1 |
(1)完全反应后生成水的质量;
(2)生成的水中氧的质量;
(3)生成的水中氢的质量;
(4)水中氢和氧的质量比.
考点:水的组成,气体的干燥(除水),氢气的化学性质与燃烧实验
专题:空气与水
分析:根据氧化铜和玻璃管的总质量的减少量是氧化铜中氧元素的质量,即水中氧元素的质量;氧化钙与U型管的总质量的增加量是生成的水的质量,再用水的质量减去氧元素的质量就是氢元素的质量.
解答:解:通过方程式可知氧化铜和玻璃管的总质量的减少量是氧化铜中氧元素的质量,又因为氧化铜中的氧元素都上了生成物水中去了,所以水中氧元素的质量为:72.8g-66.4g=6.4g;氧化钙与U型管的总质量的增加量是生成的水的质量,所以生成水的质量为:110.1g-102.9g=7.2g,所以水中氢元素的质量为:7.2g-6.4g=0.8g,所以氧、氢元素的质量比为6.4g:0.8g:8:1.
所以(1)完全反应后生成水的质量为7.2g;
(2)生成的水中氧的质量为6.4g;
(3)生成的水中氢的质量为0.8g;
(4)水中氢和氧的质量比1:8.
故答案为:(1)7.2g;(2)6.4g;(3)0.8;(4)1:8.
所以(1)完全反应后生成水的质量为7.2g;
(2)生成的水中氧的质量为6.4g;
(3)生成的水中氢的质量为0.8g;
(4)水中氢和氧的质量比1:8.
故答案为:(1)7.2g;(2)6.4g;(3)0.8;(4)1:8.
点评:解答本题的关键是要知道氧化铜和玻璃管的总质量的减少量是氧化铜中氧元素的质量;氧化钙与U型管的总质量的增加量是生成的水的质量.

练习册系列答案
相关题目
有四瓶失去标签的溶液,它们分别是:①氯化铜溶液、②稀盐酸、③硫酸钠溶液、④氢氧化钠溶液,不用其他试剂就可以将它们加以鉴别,则鉴别出来的先后顺序可能是( )
| A、①②④③ | B、①④②③ |
| C、④①②③ | D、②③①④ |
 如图所示:
如图所示: 如图是A、B两物质(均不含结晶水)的溶解曲线,据此回答以下问题:
如图是A、B两物质(均不含结晶水)的溶解曲线,据此回答以下问题: