题目内容
A、B、C、D四种化合物由下表离子中的两种构成(每种离子只能选一次).
四种化合物之间有如下反应:
①A+B→白色沉淀(不溶于硝酸) ②B+D→红褐色沉淀 ③B+C→白色沉淀(再加硝酸,沉淀转化为C)
由此推知A、B、C、D分别为A B C D .
| 阳离子 | Ba2+ | Na+ | Fe3+ | Mg2+ |
| 阴离子 | Cl- | NO3- | SO4- | OH- |
①A+B→白色沉淀(不溶于硝酸) ②B+D→红褐色沉淀 ③B+C→白色沉淀(再加硝酸,沉淀转化为C)
由此推知A、B、C、D分别为A
考点:物质的鉴别、推断,碱的化学性质,盐的化学性质
专题:常见物质的推断题
分析:根据钡离子、硫酸根离子会生成硫酸钡白色沉淀且不溶于酸,镁离子、氢氧根离子会生成氢氧化镁白色沉淀能与酸反应而溶解,氢氧根离子会与铁离子生成氢氧化铁红褐色沉淀等知识进行分析.
解答:解:沉淀离子为钡离子、硫酸根离子、氢氧根离子,①、②、③中都有B物质说明B物质为氢氧化钡,A+B→白色沉淀,不溶于硝酸,所以为Ba2+和SO42-反应生成硫酸钡沉淀,所以B是氢氧化钡,A是硫酸钠,B+D→红褐色沉淀,所以为Fe3+和OH-作用生成氢氧化铁沉淀,所以D是氯化铁,C+B→白色沉淀,再加硝酸沉淀则转化为C,可推测生成的沉淀为不溶性碱,所以C是硝酸镁,经过验证,推出的各种物质均满足题中的转化关系,推导正确,所以A是硫酸钠,B是氢氧化钡,C是硝酸镁,D是氯化铁.
故答案为:硫酸钠,氢氧化钡,硝酸镁,氯化铁.
故答案为:硫酸钠,氢氧化钡,硝酸镁,氯化铁.
点评:在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后进行验证即可.

练习册系列答案
相关题目
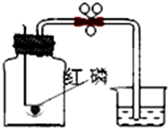 可用于测定空气中氧气的含量.实验前在集气瓶中加入少量水,并做上记号.下列说法中不正确的是( )
可用于测定空气中氧气的含量.实验前在集气瓶中加入少量水,并做上记号.下列说法中不正确的是( )| A、实验时红磷一定要过量 |
| B、点燃红磷前要先夹紧弹簧夹 |
| C、红磷熄灭后立即打开弹簧夹 |
| D、最终进入瓶中的水的体积约为氧气的体积 |
在下列实验操作(或措施)中,不正确的是( )
| A、用过氧化氢制氧气时,向过氧化氢溶液中加入少量MnO2-加快分解速率 |
| B、点燃氢气前,一定要先检验氢气的纯度-防止发生爆炸 |
| C、装NaOH溶液的试剂瓶用橡皮塞而不用玻璃塞-防止溶液变质 |
| D、实验室储存白磷时,将其浸没在冷水中-防止发生自燃 |
下列各组离子能共存的是( )
| A、H+、Na+、NO3- |
| B、Ba2+、OH-、SO42- |
| C、Ca2+、NO3-、CO32- |
| D、Ag+、Na+、Cl- |
化学变化的本质特征是( )
| A、发光 | B、发热 |
| C、产生沉淀 | D、生成新的物质 |
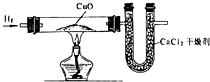 有人利用氢气还原氧化铜的实验来测定水的组成.如图得到下列结果:
有人利用氢气还原氧化铜的实验来测定水的组成.如图得到下列结果: