题目内容
14.配平下列反应的化学方程式:(1)4 Al+3 O2$\frac{\underline{\;点燃\;}}{\;}$2 Al2O3
(2)1 Fe2O3+3 CO$\frac{\underline{\;高温\;}}{\;}$2 Fe+3 CO2
(3)4 FeS+7 O2$\frac{\underline{\;高温\;}}{\;}$2 Fe2O3+4 SO2
(4)2 C6H6+15 O2$\frac{\underline{\;点燃\;}}{\;}$12 CO2+6 H2O.
分析 根据质量守恒定律:反应前后各原子的数目不变,选择相应的配平方法(最小公倍数法、定一法等)进行配平即可;配平时要注意化学计量数必须加在化学式的前面,配平过程中不能改变化学式中的下标;配平后化学计量数必须为整数.
解答 解:(1)铝和氧气在点燃的条件下生成氧化铝,然后利用最小公倍数法配平,化学方程式为:4Al+3O2$\frac{\underline{\;点燃\;}}{\;}$2Al2O3;
(2)本题可从得失氧的角度配平,一个CO分子反应中获得一个氧原子变为二氧化碳分子,由于一个Fe2O3分子中氧原子的数目为3个,所以CO与CO2前面的化学计量数都为3,最后配平其它元素的原子,Fe2O3、Fe前面的化学计量数分别为1、2;
(3)本题可利用“定一法”进行配平,把Fe2O3的化学计量数定为1,则FeS、O2、SO2前面的化学计量数分别为:2、$\frac{7}{2}$、2,同时扩大2倍,则FeS2、O2、Fe2O3、SO2前面的化学计量数分别为:4、7、2、4;
(4)本题可利用“定一法”进行配平,把C6H6的计量数定为1,CO2、H2O、O2前面的化学计量数分别为:6、3、$\frac{15}{2}$,再同时扩大2倍,则C6H6、CO2、H2O、O2前面的化学计量数分别为2、12、6、15.
故答案为:(1)4、3、2;
(2)1、3、2、3;
(3)4、7、2、4;
(4)2、15、12、6.
点评 本题难度不大,配平时化学计量数必须加在化学式的前面,配平过程中不能改变化学式中的下标;配平后化学计量数必须为整数,配平过程中若出现分数,必须把分数去分母转化为整数.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
5.图为A、B、C三种固体物质(不含结晶水)的溶解度曲线.下列说法错误的是( )
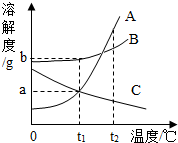

| A. | t1℃时,三种物质中B的溶解度最大 | |
| B. | t2℃时,取三种物质各a g分别放入100g水中充分溶解,只有C物质能形成饱和溶液 | |
| C. | 将等质量的三种物质的饱和溶液分别由t2℃降温到t1℃,A溶液中析出的晶体质量最大 | |
| D. | 可用降温的方法使接近饱和的C溶液变为饱和溶液 |
2.归纳总结是学习化学一种常用的方法.下列归纳总结中说法正确的是( )
①水银不是银,而是金属汞,常温常压下是液态,有毒;②铅笔芯中不含铅,主要是石墨和粘土;③干冰不是冰,而是固体二氧化碳 ④纯碱不是碱,而是一种盐.
①水银不是银,而是金属汞,常温常压下是液态,有毒;②铅笔芯中不含铅,主要是石墨和粘土;③干冰不是冰,而是固体二氧化碳 ④纯碱不是碱,而是一种盐.
| A. | ①②③④ | B. | ①②③ | C. | ②③④ | D. | ①③④ |
9.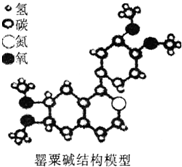 毒品是全球性公害,是人类共同的敌人.罂粟碱即是其中的一种,从组成和结构认识罂粟碱叙述正确的是( )
毒品是全球性公害,是人类共同的敌人.罂粟碱即是其中的一种,从组成和结构认识罂粟碱叙述正确的是( )
 毒品是全球性公害,是人类共同的敌人.罂粟碱即是其中的一种,从组成和结构认识罂粟碱叙述正确的是( )
毒品是全球性公害,是人类共同的敌人.罂粟碱即是其中的一种,从组成和结构认识罂粟碱叙述正确的是( )| A. | 罂粟碱是由四种原子构成的有机物 | |
| B. | 罂粟碱分子中含有4种原子 | |
| C. | 罂粟碱中氮、氧元素的质量比为1:4 | |
| D. | 罂粟碱中氢原子与碳原子的个数比为19:21 |
4.在水的电解实验中,若某电极收集到的气体是8mL,则另一个电极收集到的气体体积是( )
| A. | 4mL | B. | 16mL | C. | 4mL或16mL | D. | 8mL |
