题目内容
20.建立宏观、微观和符号之间的联系是化学学科的重要内容.(1)人类对原子的认识永无止境,道尔顿认为原子是“实心球体”,卢瑟福认为原子是“行星模型”,即原子是由带正电荷的原子核和核外电子构成.
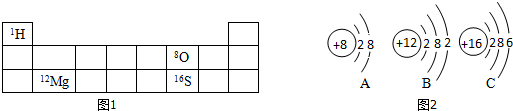
(2)图1是元素周期表的一部分(数字表示相应元素的原子序数).表中部分元素的原子(离子)结构示意图如图2,A、B、C中属于阴离子的是A(填粒子符号);在元素周期表中,氧、硫元素处于同一族(“族”或“周期”),其原因是原子的核外电子数相同;请从表中四种元素中选择组成一种酸,其化学式为H2SO4.
(3)如图3是某化学反应前后的微观过程示意图,其中“
 ”“
”“ ”表示两种不同的原子.请根据图示回答:
”表示两种不同的原子.请根据图示回答: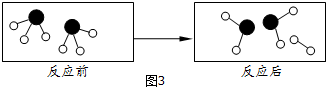
该化学反应的基本反应类型是分解反应;据图可知化学反应遵守质量守恒定律的根本原因是反应前后原子种类和数目不变.
分析 (1)根据原子是由居于原子中心的带正电的原子核和核外带负电的电子构成的进行分析;
(2)根据质子数小于核外电子数的微粒带负电,为阴离子,在元素周期表中,每一纵行称为一族,最外层电子数相等,每一横行称为一个周期,电子层数相同,四种元素中选择组成一种酸是硫酸,化学式为:H2SO4进行分析;
(3)根据化学反应前后的微观过程示意图可以看出,反应物是一种物质,生成物是两种物质,满足分解反应一变多的条件,属于分解反应,以及质量守恒定律的微观解释进行分析.
解答 解:(1)原子是由居于原子中心的带正电的原子核和核外带负电的电子构成的;
(2)质子数小于核外电子数的微粒带负电,为阴离子,A微粒的质子数小于核外电子数,B微粒的质子数等于核外电子数,C微粒的质子数大于核外电子数,所以属于阴离子的是A,在元素周期表中,每一纵行称为一族,最外层电子数相等,每一横行称为一个周期,电子层数相同,四种元素中选择组成一种酸是硫酸,化学式为:H2SO4;
(3)化学反应前后的微观过程示意图可以看出,反应物是一种物质,生成物是两种物质,满足分解反应一变多的条件,属于分解反应,化学反应遵守质量守恒定律的根本原因是反应前后原子质量和数目不变.
故答案为:(1)原子核;
(2)A,族,核外电子数,H2SO4;
(3)分解反应,原子.
点评 本题难度不大,考查了人类认识原子结构的历史、原子构成等知识,学以致用是解题的关键.

练习册系列答案
 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
2.在密闭容器中,7.2g碳与一定量氧气恰好完全反应,生成气体的质量可能是( )
| A. | 8.4g | B. | 17.8g | C. | 26.4g | D. | 44g |
15.以下叙述不正确的是( )
| A. | 钛和钛合金是制造飞机和轮船的理想材料 | |
| B. | 钙是人体中含量最多的金属元素 | |
| C. | 黄铜是铜、锌合金,它的硬度大于铜 | |
| D. | 焊锡的熔点比锡和铅都高 |
12.下列对用排水法收集满氧气的集气瓶的处理方法中,正确的是( )
| A. | 将集气瓶从水中提起后,用玻璃片盖住瓶口,然后使瓶口向上正立放在桌面上 | |
| B. | 在水下用玻璃片盖住集气瓶口后一起拿出水面,然后正立放置在桌面上 | |
| C. | 将集气瓶从水中提出后倒立放置在桌面上 | |
| D. | 将集气瓶仍然留在水槽中,用时再取出来 |
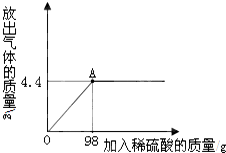 某校化学兴趣小组为了测定某一碳酸钠样品中碳酸钠的质量分数,进行如下实验,取13.25g碳酸钠样品(杂质既不溶于酸也不溶于水)放入烧杯中,加入95.8g水使其完全溶解,再向其中加入稀硫酸,测得反应放出气体的总质量与所加入稀硫酸的质量关系曲线如图所示,请根据题意解答问题:
某校化学兴趣小组为了测定某一碳酸钠样品中碳酸钠的质量分数,进行如下实验,取13.25g碳酸钠样品(杂质既不溶于酸也不溶于水)放入烧杯中,加入95.8g水使其完全溶解,再向其中加入稀硫酸,测得反应放出气体的总质量与所加入稀硫酸的质量关系曲线如图所示,请根据题意解答问题: