题目内容
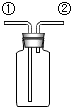
20. 根据如图装置回答下列问题:
根据如图装置回答下列问题:(1)若在锥形瓶中装有碳酸钙,则该装置可以制取的气体是二氧化碳;但是某同学在B中装入氢氧化钠溶液,最后未收集到该气体,原因是(用化学方程式表示)2NaOH+CO2=Na2CO3+H2O.
(2)若用此套装置制取干燥氧气,则锥形瓶中发生反应的化学方程式是2H2O2=2H2O+O2↑;那么B装置应该装入的物质名称是浓硫酸.
分析 (1)用碳酸钙和稀盐酸反应可以产生二氧化碳,氢氧化钠能够吸收二氧化碳;
(2)该装置适合过氧化氢溶液在二氧化锰的作用下制取氧气,浓硫酸具有吸水性,可以干燥氧气.
解答 解:(1)用碳酸钙和稀盐酸反应可以产生二氧化碳,因为氢氧化钠能够吸收二氧化碳,故最后未收集到二氧化碳,反应的方程式为:2NaOH+CO2=Na2CO3+H2O;
(2)该装置适合过氧化氢溶液在二氧化锰的作用下制取氧气,因为浓硫酸具有吸水性,可以干燥氧气,故B装置应该装入的物质名称是浓硫酸.
故答案为:(1)2NaOH+CO2=Na2CO3+H2O;
(2)浓硫酸.
点评 本题是根据装置的特点选择气体的制取、干燥、吸收等问题,难度不大,关键是明确发生装置和收集装置选择的依据.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
11.下列化学方程式错误的是( )
| A. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | B. | 2KClO3$\frac{\underline{\;MnO_2\;}}{\;}$2KCl+3O2↑ | ||
| C. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | D. | 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO |
8.下列关有机物化合物性质的叙述,错误的是( )
| A. | 大多能溶于水 | B. | 大多熔沸点低 | C. | 大多易燃烧 | D. | 大多不导电 |
9.已知12.5克石灰石样品(含杂质)完全溶解于100克稀盐酸中.测得反应过程中在不同时间的剩余物总质量如表所示:
问:(1)反应中生成了二氧化碳气体4.4克.
(2)该样品中含碳酸钙的质量分数.
| 反应时间/分 | T0 | T1 | T2 | T3 | T4 | T5 |
| 剩余质量/克 | 112.5 | 111.4 | 110.3 | 109.2 | 108.1 | 108.1 |
(2)该样品中含碳酸钙的质量分数.
10.下面对实验现象的描述中,正确的是( )
| A. | 磷燃烧时,会产生大量的白雾 | |
| B. | 镁条在空气中能剧烈燃烧,发黄光 | |
| C. | 木炭在氧气中燃烧时发出白光 | |
| D. | 氯化氢气体和氨气混合后,产生黄烟 |
 如图是化学中“有名”的装置,有如下用途:
如图是化学中“有名”的装置,有如下用途: