题目内容
8.下列关有机物化合物性质的叙述,错误的是( )| A. | 大多能溶于水 | B. | 大多熔沸点低 | C. | 大多易燃烧 | D. | 大多不导电 |
分析 根据有机化合物的共性分析解答;
解答 解:有机物的共性:熔点较低、难溶于水、受热容易分解、容易燃烧、不易导电等;故选A.
点评 本题考查有机物的性质,比较基础,旨在考查学生对基础知识的理解掌握.

练习册系列答案
相关题目
17.规范、正确的进行实验操作,是安全和成功的重要保证.下列有关实验操作,不正确的是( )
| A. | 实验剩余药品应放回原瓶,不能丢弃,也不能带出实验室 | |
| B. | 量取液体时,视线要与量筒内液体凹液面的最低处保持水平 | |
| C. | 给试管里的液体加热,液体不应超过试管溶积的1/3 | |
| D. | 实验中万一眼睛溅进药液,立即用水冲洗,必要时请医生治疗 |
16.下列四种粒子的结构示意图中,说法正确的是( )
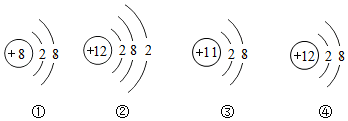

| A. | 它们表示四种不同的元素 | B. | ②在化学变化时易失两个电子 | ||
| C. | ①③④表示的元素都是非金属元素 | D. | ①④表示的是阳离子 |
3.实验室需配制2000g 2%的氢氧化钠溶液.
(1)配制时需称取氢氧化钠固体40 g,水1960 mL(水的密度取1g/cm3).
(2)用质量为23.1g的烧杯为容器,在托盘天平上称取所需的氧氧化钠固体时,请在如表中选出所需的砝码(打“√”表示选用),并在如图选出能正确表示游码位置的选项C.(填序号).表格算一格.

(1)配制时需称取氢氧化钠固体40 g,水1960 mL(水的密度取1g/cm3).
(2)用质量为23.1g的烧杯为容器,在托盘天平上称取所需的氧氧化钠固体时,请在如表中选出所需的砝码(打“√”表示选用),并在如图选出能正确表示游码位置的选项C.(填序号).表格算一格.
| 砝码大小/g | 100 | 50 | 20 | 20 | 10 | 5 |
| 打“√”表示选用 | 1 |

13. 某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:
某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:
碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入到该烧杯中,每次均充分反应.实验数据记录如下:
请你据此分析计算:
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是1.8克.
(2)该产品中碳酸钠的质量分数是否合格?
(要求写出计算过程,结果精确到0.1%)
(3)求所用盐酸的质量分数.(结果精确到0.1%)
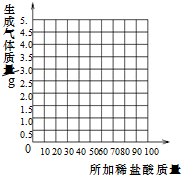
(4)根据实验数据,在右边的坐标纸上绘制出所加稀盐酸质量与生成气体质量关系的曲线.(写出必要的计算过程)
 某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:
某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入到该烧杯中,每次均充分反应.实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 烧杯及所盛物质总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是1.8克.
(2)该产品中碳酸钠的质量分数是否合格?
(要求写出计算过程,结果精确到0.1%)
(3)求所用盐酸的质量分数.(结果精确到0.1%)
(4)根据实验数据,在右边的坐标纸上绘制出所加稀盐酸质量与生成气体质量关系的曲线.(写出必要的计算过程)
18.下列物质露置于空气中,因变质而质量变大的是( )
①浓盐酸 ②石灰石 ③生石灰 ④浓硫酸 ⑤氢氧化钠.
①浓盐酸 ②石灰石 ③生石灰 ④浓硫酸 ⑤氢氧化钠.
| A. | ③⑤ | B. | ①②③⑤ | C. | ③④⑤ | D. | 全部 |
 根据如图装置回答下列问题:
根据如图装置回答下列问题: