题目内容
5.下列变化过程中,对应关系正确的是( )| A. |  稀释等质量的30%H2SO4和10% H2SO4 | |
| B. |  用等质量、等浓度的双氧水分别制取氧气 | |
| C. |  将等质量的Mg和Fe投入到足量稀H2SO4中 | |
| D. |  电解水 |
分析 A、根据酸加水稀释pH值升高考虑;
B、催化剂只能改变反应的速率,对生成物的质量没有影响;
C、根据等质量的铁和镁与足量酸反应产生氢气的多少进行判断;
D、根据电解水得到的氧气和氢气的质量比考虑.
解答 解:A、稀释等质量的30%H2SO4和10% H2SO4,浓度高的酸溶液pH值升高快,故A正确;
B、催化剂只能改变反应的速率,对生成物的质量没有影响,所以生成的氧气的质量是相等的,故B错;
C、将等质量的镁片和铁片投入到足量稀H2SO4中镁产生的氢气要比铁产生的氢气多,所以镁的曲线应该在上边,镁比铁活泼,镁应该先到达最高点,故C错;
D、电解水得到的氧气和氢气的质量比是8:1,故D错.
故选:A.
点评 解答这类题目时,首先,要知道酸碱加水稀释后pH值的变化情况,一定要理解催化剂的概念、催化作用,知道金属与酸反应产生氢气多少的判断方法,根据所给的问题情景及相关信息,结合所学的相关知识和技能,联系起来细心地探究、推理后,按照题目要求进行选择或解答即可.

练习册系列答案
相关题目
16.自来水生产中常用适量的氯气进行杀菌消毒,氯气与水反应的生成物之一是盐酸,市场上有些不法商贩为牟取暴利,用自来水冒充纯净水出售.为辨别纯净水的真伪,可用下列哪一种试剂来鉴别( )
| A. | 酚酞 | B. | BaCl2 | C. | CO2 | D. | AgNO3 |
10.溶液中的溶质是( )
| A. | 单质 | B. | 化合物 | C. | 混合物 | D. | 以上都可以 |
3.下列各项化学实验的操作中,不正确的是( )
| A. | 给烧杯中液体加热时,在烧杯下面垫上石棉网 | |
| B. | 被加热的玻璃容器外壁如有水,加热前应擦干 | |
| C. | 熄灭酒精灯只能用灯帽盖灭,不能用嘴吹、手扇等方法熄灭 | |
| D. | 用托盘天平称量物质时,先加小砝码再依次加较大的砝码 |
 取一块金属钠,用小刀切下一小块.观察到切面呈银白色,切面很快变暗,这是由于钠极易跟空气中的氧气反应生成氧化钠.把一小块金属钠投入盛有水的烧杯中,钠浮在水面上,钠与水迅速反应生成氢氧化钠和氢气,放出的热使钠熔成小球,小球在水面上滚动,发出“嗤嗤”的声响,小球越来越小,最后完全消失.
取一块金属钠,用小刀切下一小块.观察到切面呈银白色,切面很快变暗,这是由于钠极易跟空气中的氧气反应生成氧化钠.把一小块金属钠投入盛有水的烧杯中,钠浮在水面上,钠与水迅速反应生成氢氧化钠和氢气,放出的热使钠熔成小球,小球在水面上滚动,发出“嗤嗤”的声响,小球越来越小,最后完全消失.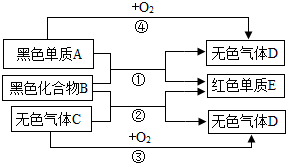 A是非金属,E是金属,B、C、D是化合物,它们之间有如下图所示的转化关系(反应条件已略去).请回答下列问题:
A是非金属,E是金属,B、C、D是化合物,它们之间有如下图所示的转化关系(反应条件已略去).请回答下列问题: 小兵在一本参考书上发现,镁居然能在二氧化碳气体中燃烧!于是他迫不及待地做起了这个实验:将镁条点燃后迅速伸入盛二氧化碳的集气瓶中,发现镁条剧烈燃烧,发出白光,放热,产生一种白色粉末和一种黑色粉末.
小兵在一本参考书上发现,镁居然能在二氧化碳气体中燃烧!于是他迫不及待地做起了这个实验:将镁条点燃后迅速伸入盛二氧化碳的集气瓶中,发现镁条剧烈燃烧,发出白光,放热,产生一种白色粉末和一种黑色粉末.