题目内容
16. 某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究.
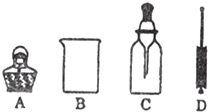
某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究.(1)如图1所示装置和药品进行实验,实验中可观察到的现象是红磷燃烧放出大量白烟,待装置冷却到室温后,打开止水夹看到烧杯中的水倒流进集气瓶,且上升到刻度“1”处,该反应的化学式表达式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)甲同学认为可用木炭代替红磷红磷测定空气中氧气的含量,乙同学 认为不可以,其原因是:木炭和氧气反应生成二氧化碳气体,装置内的压强基本不变.乙同学用图1实验装置测定的结果是:空气中氧气含量与正常值有较明显的偏差,其原因可能是(答出一种即可):装置漏气.
(3)丙同学用镁条代替红磷来测定空气中氧气的含量.结果却发现倒吸的水量远远超过集气瓶 的$\frac{1}{5}$.小组内同学帮她仔细检查,发现装置的气密性 及操作步骤均无问题.你认为造成此现象的原因可能是镁条和空气中其他成分也发生了反应.
(4)小组内同学反思上述实验的探究过程后认为:用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是:药品本身是固体,能且只能和空气中氧气反应,且生成物不是气体.
(5)小组内同学还对该实验进行了如图2改进.(已知试管容积为45mL)实验的主要操作步骤如下:
①点燃酒精灯.
②撤去酒精灯,待试管冷却后松开弹簧夹.
③将少量红磷平装入试管中,将20mL的注射器 活塞置于10mL刻度处,并按图2中所示的连接方式固定好,再将弹簧夹紧橡皮管.
④读取注射器活塞的数据.
你认为正确的实验操作顺序是③①②④(填序号).注射器活塞将从10mL刻度处慢慢前移到约为1 mL刻度处才停止.
(6)由图1实验还可推知反应后剩余气体的两点性质是:①物理性质难溶于水 ②化学性质不燃烧、不支持燃烧.
分析 本题考查的内容有常规性的实验现象的描述和化学式表达式的书写,实验误差分析,在此基础上加大了深度,分析木炭能否代替红磷以及镁带代替红磷燃烧产生的截然相反地误差的原因,这要求学生要从瓶内压强的变化去分析.对于用注射器改进后的仪器其刻度更容易读取,计算部分要注意被反应消耗掉的是试管内的氧气,不包含注射器内的部分.
解答 解:(1)红磷燃烧时生成大量白烟,装置冷却到室温后,打开止水夹看到烧杯中的水倒流进集气瓶,且上升到刻度“1”处,反应的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5
(2)用木炭代替红磷时,木炭和氧气反应生成二氧化碳气体,装置内的压强基本不变;空气中氧气含量与正常值有较明显的偏差,其原因可能是装置漏气、红磷不足、装置没冷却就打开止水夹等.
(3)镁条不但可以和氧气反应,也可以和氮气反应,所以消耗的气体的体积要大于五分之一,进入广口瓶中水的体积也会超过五分之一;
(4)根据药品与氧气反应的产物是否能够产生压强差可以知道在选择药品时要保证药品本身是固体,能且只能和空气中氧气反应,且生成物不是气体;
(5)正确的实验操作顺序是:先将少量红磷平装入试管中,将20mL的注射器活塞置于10mL刻度处,并按上图2中所示的连接方式固定好,再将弹簧夹紧橡皮管,再点燃酒精灯,再撤去酒精灯,待试管冷却后松开弹簧夹,最后读取注射器活塞的数据,即顺序是③①②④;
因为试管容积为45mL,所以试管中氧气的体积为45mL×$\frac{1}{5}$=9mL,待试管冷却后松开弹簧夹,注射器活塞将从10mL刻度处慢慢前移到约为1mL刻度处才停止.
(6)由于烧杯中的水倒流进集气瓶,且上升到刻度“1”处,而不是全部,说明剩余的气体具有难溶于水的物理性质,不燃烧、不支持燃烧的化学性质.
故答案为:
(1)红磷燃烧放出大量白烟;烧杯中的水倒流进集气瓶,且上升到刻度“1”处;4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(2)木炭和氧气反应生成二氧化碳气体,装置内的压强基本不变;装置漏气;
(3)镁条和空气中其他成分也发生了反应;
(4)药品本身是固体,能且只能和空气中氧气反应,且生成物不是气体;
(5)③①②④;1;
(6)难溶于水;不燃烧、不支持燃烧.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

 中考解读考点精练系列答案
中考解读考点精练系列答案| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | / |
| 熔点/℃ | / | / | 1535 |
| A. | 铁丝在氧气里燃烧时产生火星四射现象 | |
| B. | 可以用稀盐酸验证球状物质中含有铁 | |
| C. | 铁丝燃烧时温度高于1400℃而低于1535℃ | |
| D. | Fe3O4中铁元素具有两种化合价 |
(1)小明查阅资料得知镁能与稀盐酸反应,该反应属于的基本反应类型是置换反应.
(2)他取一支试管,放入一根镁条,加入一定量硫酸铜溶液,观察到镁条表面有少量气泡产生,且有黑色物质生成.镁条与硫酸铜溶液反应的现象让小明感到困惑,他去图书馆查到相关资料:
资料1:硫酸铜溶液在配制时加入了少量硫酸;
资料2:当金属粉末颗粒很小时,容易成为黑色;
资料3:实验过程中发生了一系列复杂的反应,生成的黑色粉末可能是CuO、Cu中的一种或两种.
①镁条与硫酸铜溶液反应的实验中产生的气体可能为H2(填化学式).
②小明进一步设计实验确定黑色粉末的成分,请在下表中补全实验方案.
| 实验操作 | 实验现象 | 结论 |
| 将黑色粉末过滤、晾干后,分成两份 | ||
| 将其中一份装入硬质玻璃管中,向其中通入CO后,加热,并将生成的气体通入澄清石灰水中 | 澄清石灰水 变浑浊 | 结论I |
| 将另一份置于坩埚中,称其质量为m1,在空气中加热一段时间后冷却,称其质量为m2. | 现象I | 黑色粉末中含Cu |
| A. | 常温下,碱溶液的pH一定大于7,盐溶液的pH一定等于7 | |
| B. | 钢质车架主要是用合成材料制成的 | |
| C. | 区别NH4Cl和KCl粉末,可用分别加熟石灰研磨并闻气味的方法 | |
| D. | Na2CO3俗称纯碱,它的水溶液呈碱性,属于碱类 |
| A. | H2SO4 NaCl Na2CO3 CaCl2 | B. | HCl NaOH CuSO4Mg SO4 | ||
| C. | Na2CO3 K2SO4 BaCl2 HCl | D. | NaNO3 HCl CaCl2 KOH |