题目内容
2.化学是以实验为基础的自然科学,如图所示为实验室常用的实验装置: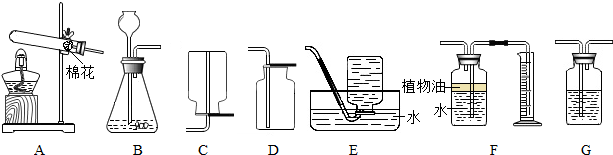
据此回答:
(1)实验室若用A装置制取氧气,写出反应的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(2)B装置可以用来制取O2、H2,还可以用来制取二氧化碳,反应的方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,F装置可用来测量生成该气体的体积,其中在水面上放一层植物油的目的是防止二氧化碳溶于水,植物油上方的空气对实验结果没有影响(选填“有”或“没有”)(瓶中水的体积大于测量气体的体积).
(3)实验室若收集干燥的O2,应将气体通过G装置,瓶内装入的物质是浓硫酸,气体应该从左端(选填“左“或”右“)通入.
分析 (1)根据高锰酸钾是固体,反应条件是加热,故选择发生装置A解答;
(2)根据实验室制取二氧化碳的原理解答;根据二氧化碳的性质能溶于水进行解答.
(3)根据浓硫酸具有吸水性,常用作气体的干燥剂解答.
解答 解:(1)实验室若用A装置制取氧气属于固故加热型,可以用高锰酸钾制氧气,反应的方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)B装置是固液常温型,可以用来制取O2、H2,还可以用来制取二氧化碳,方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,要测量二氧化碳的体积只能用排水法,用量筒测量水的体积从而测二氧化碳的体积;二氧化碳能溶于水,所以要在水的上方放一层植物油.油上方的空气对实验结果没有影响.
(3)浓硫酸具有吸水性,常用作气体的干燥剂.气体应该从左端进入.
故答案为:
(1)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,A; C或E;
(2)二氧化碳;CaCO3+2HCl=CaCl2+H2O+CO2↑,防止二氧化碳溶于水,没有;
(3)浓硫酸;左.
点评 本题要根据制取气体发生装置和收集装置选择依据进行装置选择;易错点在植物油的作用及上方空气对实验结果有没有影响,考查学生利用知识分析问题的能力.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
10.不用其他试剂无法鉴别的是( )
| A. | H2SO4 NaCl Na2CO3 CaCl2 | B. | HCl NaOH CuSO4 MgSO4 | ||
| C. | Na2CO3 K2SO4 BaCl2 HCl | D. | NaNO3 HCl CaCl2 KOH |
17.保护环境就是善待自己,造福人类,下列做法不合理的是( )
| A. | 为减少环境污染,关闭所有的化工厂 | |
| B. | 农村推广使用沼气、太阳能等清洁能源,减少使用煤、柴火等传统燃料 | |
| C. | 减少使用化肥,推广使用农家肥 | |
| D. | 城市生活提出五公里以内出行,骑自行车或乘坐公共交通工具 |
7.小芳同学从超市购买了一瓶维生素C泡腾片.下图是维生素C泡腾片标签上的部分内容:
小芳同学根据使用说明将维生素C泡腾片放入一杯水中,发现维生素C泡腾片逐渐溶解,产生大量气泡,片刻后变成为一杯鲜甜的橙味饮品.小芳同学感到很好奇,产生的气泡是什么?请参与小芳同学的探究:【提出问题】维生素C泡腾片放入水中,产生的气泡是什么呢?
【我的猜想】气体成分是二氧化碳,理由是成分中含有碳酸氢钠和酒石酸,碳酸氢钠能和显酸性的物质反应生成二氧化碳气体.
【实验方案】
根据维生素C泡腾片储存条件,请说明保存时要低温和防潮的原因是:
①维生素C泡腾片热稳定性差;
②维生素C泡腾片溶于水时能够发生化学反应.
| 维生素C泡腾片 功能:补充人体维生素C,增强机体抵抗力 主要成分:维生素C, 辅料成分:碳酸氢钠、氯化钠、酒石酸晶体、蔗糖、 糖精钠、阿朴胡萝卜醛、橘味香精、橙味香精、维生素B 贮藏:低温、避光、防潮 |
【我的猜想】气体成分是二氧化碳,理由是成分中含有碳酸氢钠和酒石酸,碳酸氢钠能和显酸性的物质反应生成二氧化碳气体.
【实验方案】
| 实验步骤 | 实验现象 | 实验结论 |
| 将一片维生素C泡腾片放入水中,将产生的气体通入 澄清石灰水中 | 澄清石灰水变浑浊 | 气体是二氧化碳 |
①维生素C泡腾片热稳定性差;
②维生素C泡腾片溶于水时能够发生化学反应.
14.做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你与他们一起进行以下探究.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】
(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质是Na2SO4和H2SO4两种物质.
(3)丙同学认为溶液中的溶质是Na2SO4和NaOH两种物质.
【查阅资料】
①Na2SO4溶液呈中性
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)等物质.
【总结反思】丁同学根据乙、丙两位同学的实验现象,首先肯定猜想(1)不成立.经过进一步分析,丁同学认为猜想(2)也不成立,他的理由是滴入酚酞试液后,溶液变红色,说明溶液呈碱性,溶液中不可能含有硫酸.兴趣小组的同学经过充分讨论一致认为猜想(3)成立.
【知识拓展】(1)生活中能否用铝制品来盛放强碱性溶液?不能(填“能”或“不能”)
(2)乙同学的实验中铝片与氢氧化钠溶液发生了反应,请写出铝与该溶液发生反应的化学方程式2Al+2NaOH+2H2O═2NaAlO2+3H2↑..
【提出问题】溶液中的溶质是什么物质?
【作出猜想】
(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质是Na2SO4和H2SO4两种物质.
(3)丙同学认为溶液中的溶质是Na2SO4和NaOH两种物质.
【查阅资料】
①Na2SO4溶液呈中性
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)等物质.
| 实验操作 | 实验现象 | 实验结论 | |
| 乙同学 实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想(2)成立 |
| 丙同学 实验 | 取中和反应后的溶液少许于试管中,向试管中滴加几滴无色酚酞试液 | 溶液变红红色 | 猜想(3)成立 |
【知识拓展】(1)生活中能否用铝制品来盛放强碱性溶液?不能(填“能”或“不能”)
(2)乙同学的实验中铝片与氢氧化钠溶液发生了反应,请写出铝与该溶液发生反应的化学方程式2Al+2NaOH+2H2O═2NaAlO2+3H2↑..
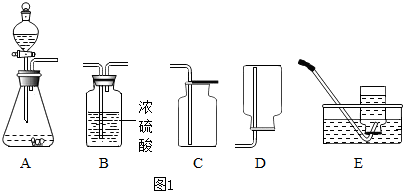
4.如图为实验室常见气体的制备和进行性质实验的部分仪器,某校化学实验探究小组的同学就用它们完成各自的探究实验,根据探究过程回答下列问题:
(1)第一小组的同学根据图1提供的仪器,制备并收集气体:
①A装置能用来制取常见的一些气体,请你写出其中的一个化学反应方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
②要制备并收集一瓶干燥、纯净的氧气,所选仪器的连接顺序为ABC(填仪器序号字母).
③聪聪同学认为只能选用C装置收集CO2,原因是二氧化碳能溶于水,密度比空气的大.
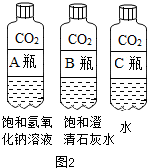
(2)第二小组的同学用干燥、纯净的CO2气体探究其化学性质:
①如图2所示,分别向盛满二氧化碳的A、B、C三个塑料瓶中,导入等体积的饱和氢氧化钠溶液、饱和澄清石灰水、水、盖紧瓶塞,充分振荡,发现:三个塑料瓶变瘪的程度为A>B>C,因此,要吸收大量CO2气体,最好选用氢氧化钠.同学们还发现,B瓶内液体出现白色浑浊,且溶液质量减小,请简述溶液质量减小的原因二氧化碳和澄清的石灰水反应,生成碳酸钙沉淀和水,故B瓶内液体出现白色浑浊,且溶液质量减小.此时,瓶内溶液pH与反应前溶液相比较是减小(填“增大”、“减小”、“不变”之一).
②阳阳同学用试管取了少量C瓶所得的液体,滴入紫色石蕊试液,紫色石蕊试液变红,原因是(用化学方程式解释)CO2+H2O=H2CO3.
| 气体制备仪器 | 气体性质仪器 |
 |  |
①A装置能用来制取常见的一些气体,请你写出其中的一个化学反应方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
②要制备并收集一瓶干燥、纯净的氧气,所选仪器的连接顺序为ABC(填仪器序号字母).
③聪聪同学认为只能选用C装置收集CO2,原因是二氧化碳能溶于水,密度比空气的大.
(2)第二小组的同学用干燥、纯净的CO2气体探究其化学性质:
①如图2所示,分别向盛满二氧化碳的A、B、C三个塑料瓶中,导入等体积的饱和氢氧化钠溶液、饱和澄清石灰水、水、盖紧瓶塞,充分振荡,发现:三个塑料瓶变瘪的程度为A>B>C,因此,要吸收大量CO2气体,最好选用氢氧化钠.同学们还发现,B瓶内液体出现白色浑浊,且溶液质量减小,请简述溶液质量减小的原因二氧化碳和澄清的石灰水反应,生成碳酸钙沉淀和水,故B瓶内液体出现白色浑浊,且溶液质量减小.此时,瓶内溶液pH与反应前溶液相比较是减小(填“增大”、“减小”、“不变”之一).
②阳阳同学用试管取了少量C瓶所得的液体,滴入紫色石蕊试液,紫色石蕊试液变红,原因是(用化学方程式解释)CO2+H2O=H2CO3.
