题目内容
4.如图为实验室常见气体的制备和进行性质实验的部分仪器,某校化学实验探究小组的同学就用它们完成各自的探究实验,根据探究过程回答下列问题:| 气体制备仪器 | 气体性质仪器 |
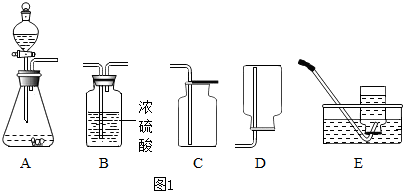 |  |
①A装置能用来制取常见的一些气体,请你写出其中的一个化学反应方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
②要制备并收集一瓶干燥、纯净的氧气,所选仪器的连接顺序为ABC(填仪器序号字母).
③聪聪同学认为只能选用C装置收集CO2,原因是二氧化碳能溶于水,密度比空气的大.
(2)第二小组的同学用干燥、纯净的CO2气体探究其化学性质:
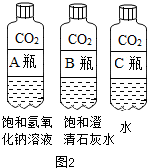
①如图2所示,分别向盛满二氧化碳的A、B、C三个塑料瓶中,导入等体积的饱和氢氧化钠溶液、饱和澄清石灰水、水、盖紧瓶塞,充分振荡,发现:三个塑料瓶变瘪的程度为A>B>C,因此,要吸收大量CO2气体,最好选用氢氧化钠.同学们还发现,B瓶内液体出现白色浑浊,且溶液质量减小,请简述溶液质量减小的原因二氧化碳和澄清的石灰水反应,生成碳酸钙沉淀和水,故B瓶内液体出现白色浑浊,且溶液质量减小.此时,瓶内溶液pH与反应前溶液相比较是减小(填“增大”、“减小”、“不变”之一).
②阳阳同学用试管取了少量C瓶所得的液体,滴入紫色石蕊试液,紫色石蕊试液变红,原因是(用化学方程式解释)CO2+H2O=H2CO3.
分析 (1)
①根据A装置是固体和液体反应不加热,可以制取氧气解答;
②根据浓硫酸具有吸水性,可以做干燥剂,排空气法收集收集的较干燥解答;
③根据二氧化碳能溶于水,只能用向上排空气法收集解答;
(2)①根据二氧化碳易于碱性溶液发生反应解答;
②根据二氧化碳能与水反应生成碳酸,碳酸能使紫色石蕊变红结案的
解答 解:
(1)
①A装置适合用于反应物是固体和液体,反应条件是常温,适合于过氧化氢制取氧气,反应的方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
②浓硫酸具有吸水性,可以做干燥剂,排空气法收集收集的较干燥,要制备并收集一瓶干燥、纯净的氧气,所选仪器的连接顺序为ABC;
③二氧化碳易溶于水,密度比空气的大,只能用向上排空气法收集;
(2)①分别向盛满二氧化碳的A、B、C三个塑料瓶中,导入等体积的饱和氢氧化钠溶液、饱和澄清石灰水、水、盖紧瓶塞,充分振荡,发现:三个塑料瓶变瘪的程度为A>B>C,因此,要吸收大量CO2气体,最好选用氢氧化钠溶液;
二氧化碳和澄清的石灰水反应,生成碳酸钙沉淀和水,故B瓶内液体出现白色浑浊,且溶液质量减小;
此时,瓶内溶液碱性减弱,pH与反应前溶液相比较是减小;
②将二氧化碳气体通入紫色石蕊试液,石蕊试液很快变红色,原因是:CO2+H2O=H2CO3;
答案:
(1)①2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;②ABC;③二氧化碳能溶于水,密度比空气的大;
(2)①氢氧化钠溶液;二氧化碳和澄清的石灰水反应,生成碳酸钙沉淀和水,故B瓶内液体出现白色浑浊,且溶液质量减小;减少;
②CO2+H2O=H2CO3;
点评 本考点主要考查气体的制取装置和收集装置、干燥装置的选择及作用,同时也考查了化学方程式的书写,综合性比较强.通过本题学生应认识到一套装置可以制取多种气体,应注意反应原理的相似之处来解答.

 阅读快车系列答案
阅读快车系列答案| A. | 氮气不与任何物质反应 | |
| B. | 洗涤剂清除油污-洗涤剂能溶解油污 | |
| C. | 水是由氢元素和氧元素组成的化合物 | |
| D. | 纯牛奶中不含任何化学物质 |
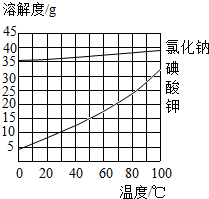 “食盐加碘”通常是在氯化钠中加入碘酸钾.如图是氯化钠和碘酸钾的溶解度曲线图.下列说法错误的是( )
“食盐加碘”通常是在氯化钠中加入碘酸钾.如图是氯化钠和碘酸钾的溶解度曲线图.下列说法错误的是( )| A. | 氯化钠易溶于水 | |
| B. | 碘酸钾的溶解度随温度升高而增大 | |
| C. | 20℃时不可能制得相同质量分数的碘酸钾溶液和氯化钠溶液 | |
| D. | 20℃时两者的饱和溶液,氯化钠的质量分数大 |
| 选项 | X | Y | Z |
| A | CO2 | Ca(OH)2溶液 | H2O |
| B | Ba(NO3)2溶液 | 稀硫酸 | Na2CO3溶液 |
| C | Al | O2 | Mg(NO3)2 |
| D | Fe2O3 | 稀盐酸 | CO |
| A. | A | B. | B | C. | C | D. | D |
| A. | 单质 | B. | 元素 | C. | 原子 | D. | 分子 |
 当前,一次性筷子、一次性饭盒的安全问题受到社会关注.专家介绍说,正规的一次性筷子所用的原料都是质地较好的木材,不需特殊加工.但是很多小作坊为了降低成本,使用劣质木材,为了使筷子看上去更白、更新,他们常用硫磺熏制漂白,结果造成SO2严重超标,同时硫磺中含有铅、汞等重金属,也会造成人体铅中毒或汞中毒.
当前,一次性筷子、一次性饭盒的安全问题受到社会关注.专家介绍说,正规的一次性筷子所用的原料都是质地较好的木材,不需特殊加工.但是很多小作坊为了降低成本,使用劣质木材,为了使筷子看上去更白、更新,他们常用硫磺熏制漂白,结果造成SO2严重超标,同时硫磺中含有铅、汞等重金属,也会造成人体铅中毒或汞中毒.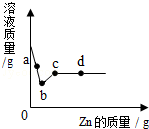 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入金属Zn,溶液质量与加入Zn的质量关系如图所示,下列叙述中不正确的说法有( )
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入金属Zn,溶液质量与加入Zn的质量关系如图所示,下列叙述中不正确的说法有( )