题目内容
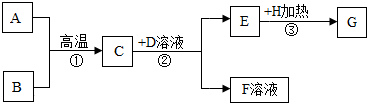
14.某化学兴趣小组的同学在做“木炭还原氧化铜”实验时,进行如下探究,实验装置如图甲图所示(假设木炭粉中不含其它杂质).
(1)刚开始预热时,试管②中立即产生气泡,但石灰水不变浑浊,原因是开始排出的是试管内的空气;
(2)继续加热,观察到试管②中澄清石灰水逐渐变浑浊,试管①中黑色粉末中出现红色物质.请你写出其中的一个化学方程式C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;
(3)充分反应后,观察到试管①中的剩余固体中仍渗杂有少量黑色固体,为了确定该黑色固体的成分,同学们进行了如下探究活动,请你帮他们完成下表:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量反应后的试管①中的固体于洁净试管内,滴入稀硫酸稀硫酸 微热. | A | 该黑色固体是木炭 |
| B | 该黑色固体是氧化铜 |
(4)有同学提出,图甲所示该实验装置存在不足,并设计了图乙所示实验装置替代图甲中试管②部分.图乙中气球的作用是收集尾气,防止一氧化碳对大气的污染收集尾气,防止一氧化碳对大气的污染;试管③的作用是防倒吸.
分析 (1)根据试管中有空气,受热时易膨胀分析;
(2)根据碳能与氧化铜反应生成铜和二氧化碳,二氧化碳能使澄清的石灰水变浑浊,写出反应的方程式;
(3)根据木炭、氧化铜与硫酸的反应分析;
(4)根据一氧化碳是对大气有污染的气体分析,加入试管③可以有效地防止倒吸.
解答 解:(1)由于试管中有空气,受热时易膨胀,所以,开始加热时排出的是试管中的空气;
(2)在高温时,碳能与氧化铜反应生成铜和二氧化碳,二氧化碳能与氢氧化钙反应生成碳酸钙沉淀和水,反应的方程式是:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑,CO2+Ca(OH)2═CaCO3↓+H2O;
(3)由于木炭不能与硫酸反应、氧化铜与硫酸反应.所以,为了确定该黑色固体的成分,同学们进行了如下探究活动为:取少量反应后的试管①中的固体于洁净试管内,滴入稀硫酸,微热.若无现象,则该黑色固体是木炭;若黑色粉末溶解,溶液由无色逐渐变为蓝色,则该黑色固体是氧化铜;
(4)由于在高温时,碳能与氧化铜反应中会产生一氧化碳,一氧化碳对大气有污染.所以,图乙中气球的作用是:收集尾气,防止一氧化碳对大气的污染.加入试管③可以有效地防止倒吸,防止试管炸裂.
故答为:(1)开始排出的是试管内的空气;
(2)C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑(或CO2+Ca(OH)2═CaCO3↓+H2O);
(3)A黑色粉末溶解;B溶液由无色逐渐变为蓝色;
(4)收集尾气,防止一氧化碳对大气的污染;防倒吸.
点评 本题是对碳还原氧化铜的实验和实验操作的综合考查,注意类似知识的迁移和灵活运用就能较快解答本题.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
2.分类法是一种行之有效、简单易行的科学方法.某同学用下表对所学知识进行分类,其中甲与乙、丙、丁是包含关系.下列各组中,有错误的组合是( )
| 选项 | 甲 | 乙、丙、丁 |
| A | 常见干燥剂 | 浓硫酸、生石灰、氢氧化钠(固体) |
| B | 常见碱 | 烧碱、纯碱、熟石灰 |
| C | 常见营养物质 | 蛋白质、维生素、无机盐 |
| D | 常见除油污的物质 | 洗洁精、汽油、氢氧化钠 |
| A. | A | B. | B | C. | C | D. | D |
19.已知某两种物质在光照条件下能发生化学反应,其微观示意图如下:(说明:一种小球代表一种元素的原子)则下列说法中正确的是( )
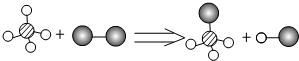
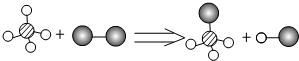
| A. | 该图示不符合质量守恒定律 | B. | 该反应属于置换反应 | ||
| C. | 图示中只有一种化合物 | D. | 该反应中分子个数比1:1:1:1 |
6.下列实验操作正确的是( )
| A. | 将氢氧化钠固体放在滤纸上称量 | |
| B. | 用10mL量筒量取8.58mL蒸馏水 | |
| C. | 氯化钠、硝酸银、碳酸钠三种无色溶液可以用稀盐酸来鉴别 | |
| D. | 制取氧气时,用二氧化锰与过氧化氢溶液在常温下反应,并用向下排空气法收集 |
1.下列变化中,一定发生化学变化的是( )
| A. | 西瓜榨成西瓜汁 | B. | 工业上分离液态空气制取氧气 | ||
| C. | 蜡烛融化成蜡油 | D. | 牛奶变酸 |