题目内容
12.下图为某化工企业生产流程示意图,请回答下列问题:
(1)钛酸亚铁(FeTiO3)中钛元素的化合价为+4,
(2)①中反应为2FeTiO3+6C+7Cl2$\frac{\underline{\;一定条件\;}}{\;}$2x+2TiCl4+6CO,则x的化学式为FeCl3,
(3)②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为7:1.
分析 (1)根据化合价代数和为零进行分析;
(2)根据质量守恒定律进行分析;
(3)根据氢气和一氧化碳反应的方程式考虑质量比.
解答 解:(1)设FeTiO3中P的化合价是x.FeTiO3中Fe的化合价是+2价,O的化合价是-2价,利用化合物中各元素的化合价的代数和为零的原则得到方程(+2)+x+(-2)×3=0解得,x=+4 所以钛酸亚铁(FeTiO3)中钛元素的化合价是+4价;
(2)根据质量守恒定律,在反应前后各元素原子的个数不变.从2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO看钛原子、氧原子、碳原子反应前后除物质x外个数已经相等,故x中无钛原子、氧原子、碳原子.铁反应前共有2个,反应后只有x有,所以2x中有2个,从而x中有1个;氯原子反应前有14个,反应后x除外有8个,所以2x中有6个,因此x中有3个,因此x的化学式是FeCl3;
(3)根据从化学方程式2H2+CO═CH3OH
4 28
由此可知一氧化碳和氢气的质量比是:28:4=7:1;
故答案为:(1)+4;
(2)FeCl3;
(3)7:1.
点评 本题主要考查了化合价的计算、化学方程式的书写以及质量守恒定律的应用,同时考查了学生从题目中获取信息并运用的能力.计算元素的化合价时一定要注意,一定不要忘记填上正号.

练习册系列答案
相关题目
2.下列说法、方程式以及基本反应类型均正确的是( )
| A. | 工业制二氧化碳 CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ 分解反应 | |
| B. | 生石灰在空气中质量增加 CaO+CO2═CaCO3+H2O 复分解反应 | |
| C. | 用木炭还原氧化铜 C+2CuO$\frac{\underline{\;高温\;}}{\;}$CO2↑+Cu 氧化反应 | |
| D. | 木炭用作燃料 C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2↑ 化合反应 |
20.在浓硫酸的催化作用下,固体草酸(H2C2O4)受热分解成碳的氧化物和水.某化学课外兴趣小组对生成物中碳的氧化物的成分进行了如下实验探究.
【提出问题】生成物中有哪种碳的氧化物?.
【猜想】
【设计实验】基于猜想3,依据CO和CO2的性质,兴趣小组同学设计了如图实验装置:
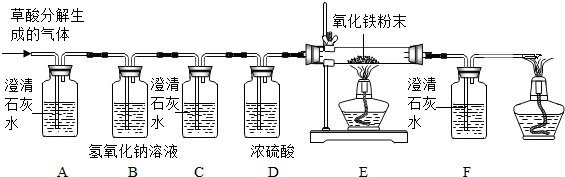
【实验探究】
(1)观察到A装置(填字母)中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成.
(2)有两种实验现象都能分别证明草酸分解的气体中含有CO:①C装置中澄清石灰水不变浑浊,F装置中澄清石灰水变浑浊;②E装置中出现红色粉末变黑色的现象;.
【实验结论】通过实验探究证明:猜想3成立.
【问题讨论】
(1)C装置的作用是检验二氧化碳是否被完全吸收;D装置的作用是吸收水分.
(2)装置末端酒精灯的作用是处理尾气CO,防止污染空气.
【提出问题】生成物中有哪种碳的氧化物?.
【猜想】
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO | 只有CO2 | 含有CO和CO2 |

【实验探究】
(1)观察到A装置(填字母)中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成.
(2)有两种实验现象都能分别证明草酸分解的气体中含有CO:①C装置中澄清石灰水不变浑浊,F装置中澄清石灰水变浑浊;②E装置中出现红色粉末变黑色的现象;.
【实验结论】通过实验探究证明:猜想3成立.
【问题讨论】
(1)C装置的作用是检验二氧化碳是否被完全吸收;D装置的作用是吸收水分.
(2)装置末端酒精灯的作用是处理尾气CO,防止污染空气.
7.化学中常常出现“1+1≠2”的有趣现象,但也有例外,下列符合“1+1=2”事实的是( )
| A. | 20℃,1 L水与1 L酒精混合后的体积等于2 L | |
| B. | 1 g镁和1 g稀硫酸充分反应后所得的溶液质量为2 g | |
| C. | 1 g硫粉在1 g氧气中完全燃烧后生成2 g二氧化硫 | |
| D. | 20℃,1 g硝酸钾饱和溶液中加入1 g硝酸钾固体能得到2 g硝酸钾溶液 |
17.下列清除污垢的过程中,发生乳化现象的是( )
| A. | 用汽油清洗油污 | B. | 用洗涤剂清洗油污 | ||
| C. | 用稀硫酸清除铁锈 | D. | 用白醋清除水垢 |
4.某钾肥的主要成分是氯化钾.称取16g该钾肥样品溶于水,加入340g质量分数为10%的硝酸银溶液恰好完全反应,反应的方程式为:KCl+AgNO3═AgCl↓+KNO3(其他成分不含钾,且不参加反应).计算:
(1)340g质量分数为10%的硝酸银溶液中硝酸银的质量.
(2)该钾肥样品中氯化钾的质量.
(3)钾肥产品的等级使用氧化钾的含量作为标准的(如下表),计算并确定该钾肥的等级.
(1)340g质量分数为10%的硝酸银溶液中硝酸银的质量.
(2)该钾肥样品中氯化钾的质量.
(3)钾肥产品的等级使用氧化钾的含量作为标准的(如下表),计算并确定该钾肥的等级.
| 钾肥的等级 | 合格 | 一等 | 优等 |
| 氧化钾的质量分数x | 54%≤x<57% | 57%≤x<60% | 60%≤x |
1.以科学原理和实验事实为依据进行推理是学习化学的一种重要方法,但盲目类推又可能得出错误结论,以下类推正确的是( )
| A. | 物质都是由元素组成的,同种元素可以组成纯净物,则不同种元素也可以组成纯净物 | |
| B. | 金属锌能与氯化铜溶液发生置换反应,所以置换反应只能发生在金属与金属的化合物之间 | |
| C. | 原子和分子均是微观粒子,在化学变化中原子不能再分,则分子也不能再分 | |
| D. | 因为某物质的溶液呈酸性,所以该物质属于酸 |
20.生活中的下列现象不属于化学变化的是( )
| A. | 蜡烛燃烧 | B. | 牛奶变酸 | C. | 燃放鞭炮 | D. | 蔬菜榨汁 |
